老化ストレス応答研究プロジェクトチームHPへようこそ
老化は、DNA傷害応答や、酸化ストレスに対応するレドックスストレス応答、組織損傷に対応した炎症ストレス応答等、種々の環境ストレスに対する適応力の低下と密接に関連する事が示唆されています。老化過程でこのようなストレス(老化ストレス)に対応した多様なシステム応答機構がどのように加齢変化するのか、あるいはどのように細胞や組織を保護するのかといった老化ストレス応答の機構研究は老化の要因や老化のメカニズムを解明する上で極めて重要な課題と考えられます。本研究プロジェクトチームでは、特にエネルギー代謝や活性酸素産生の中核オルガネラであるミトコンドリアに着目し、ミトコンドリア機能低下から始まるミトコンドリアストレス応答機構の解明を目指すとともに、細胞核への情報伝達とエピゲノム変化につながる分子機構解明を行っています。
お知らせ
オープンアクセス論文のInternational Journal of Molecular Sciences誌(IF = 6.208)に老化に関連する特集企画を立ち上げました。原著論文や総説を募集しています。投稿をお待ちしています。
Special Issue "Molecular Research of Aging Stress Respnse "
News
-
令和6年1月19-20日 第20回ファンクショナルフード学会学術集会(米子)にて清水PLおよび澁谷研究員が口頭発表を行いました。清水「Functional Food Research, Yesterday and Today」、澁谷「細胞外マトリックス制御による老化様皮膚病態の改善作用」また、澁谷研究員が本大会で、令和5年度優秀論文賞を受賞しました。「筋疲労モデルマウスを用いた運動機能改善物質の探索」NEW!
-
令和6年1月12日 東京都健康長寿医療センター研究所・老化神経生物学の西宗裕史先生を講師としてお招きしGSRCセミナーを開催しました。「筋委縮性側索硬化症(ALS)の治療を目指した神経筋接合部の研究」NEW!
-
令和5年12月12日 富山大学学術研究部薬学・和漢系 薬物治療学研究室の泉尾直孝先生を講師としてお招きしGSRCセミナーを開催しました。「中枢神経疾患における脳-末梢組織連関の解明と治療・診断への応用」
-
令和5年12月6-8日 第46回日本分子生物学会年会(神戸)にて清水PLがオーガナイザーとしてシンポジウム「ジェロサイエンス」を開催しました。また、澁谷・渡辺研究員が発表を行いました。澁谷「MMP2制御はSOD1欠損が誘導する老化様皮膚萎縮を改善する」、渡辺「ミトコンドリアストレス応答によるATF4活性化が骨細胞の核形態不全を誘導して骨量減少を起こす」
-
令和5年10月12日 清水プロジェクトリーダーが担当した研究紹介コラムが当センターHPに掲載されました。是非ご覧ください。
「早老症を知っていますか?」
- 令和5年10月11日 富山大学学術研究部薬学・和漢系 薬物治療学研究室の泉尾直孝助教授と当研究室の清水孝彦プロジェクトリーダーらの共同研究により、インスリン抵抗性が持続的な高血糖とは無関係にアルツハイマー病における記憶障害を早期発症させることを動物実験で実証し、英文学術誌「Aging Cell」で発表しました。「Insulin resistance induces earlier initiation of cognitive dysfunction mediated by cholinergic deregulation in a mouse model of Alzheimer’s disease」
 本研究の成果は10月16日に富山大学と共同でプレスリリースを行いました。富山大学プレスリリース
本研究の成果は10月16日に富山大学と共同でプレスリリースを行いました。富山大学プレスリリース 、国立長寿医療センタープレスリリース
、国立長寿医療センタープレスリリース
- 令和5年10月10日 山陽小野田市立山口東京理科大学 薬学部・再生医療学分野の嶋本顕先生を講師としてお招きしGSRCセミナーを開催しました。「ヒト老化モデルとしてのウェルナー症候群を検証する」
- 令和5年9月25日 朝日大学歯学部 口腔構造機能発育学講座・口腔解剖学の寺嶋雅彦先生を講師としてお招きしGSRCセミナーを開催しました。「コラーゲンの翻訳語修飾の異常と様々な疾患の関連性」
- 令和5年8月24日 第8回NCGGサマーリサーチセミナーにおいて澁谷研究員がポスター発表を行いました。「低栄養マーカーを改善する機能性物質の解析」
- 令和5年8月1日 お茶の水女子大学 基幹研究院自然科学系の清水誠先生を講師としてお招きしGSRCセミナーを開催しました。「繊維芽細胞増殖因子による骨格筋恒常性の制御機構」
- 令和5年7月26日 順天堂大学大学院医学研究科 整形外科・運動器医学の野尻英俊先生を講師としてお招きしGSRCセミナーを開催しました。「高齢者の脊椎疾患はどのように治療されているか?~脊椎の変性と脊柱の変形~」
- 令和5年7月13-15日 Japan Society for Biomedical Gerontology, Korea-Japan joint symposium(Seoul)において澁谷研究員が口頭発表を行いました。「Elucidation of the onsetmechanism of premature aging using novel Werner's syndrome model mice」
- 令和5年度6月12-14日 IAGG Asia/Oceania Regional Congress 2023(Yokohama)において、清水PL、澁谷・渡辺研究員がポスター発表を行いました。
- 令和5年6月9-11日 第23回日本抗加齢医学会総会(東京)のシンポジウムにおいて清水PLが口頭発表を行いました。
- 令和5年 5月9日 メンバーを更新しました。
- 令和5年 4月22日 第31回日本医学会総会(東京)の6NCリトリートポスターセッションにおいて澁谷研究員が発表を行いました。「新規ウェルナー早老症モデルマウスの老化病態解析」
【過去のNEWS】
- 令和5年 3月14-17日 日本農芸化学会2023年度大会(オンライン)のシンポジウムにおいて澁谷研究員が口頭発表を行いました。「アサイー果実抽出物は腎低酸素化を介して造血因子erythropoietinを増加する」
- 令和5年 3月3-5日 第9回骨格筋生物学研究会(神奈川)において澁谷研究員が口頭発表を行いました。「速筋ミトコンドリアROSは可逆的にグリコーゲン代謝及び運動機能を調節する」
- 令和5年 2月20日 産業技術総合研究所 細胞分子工学研究部門の小笠原理紀先生を講師としてお招きしGSRCセミナーを開催しました。「骨格筋の運動適応と加齢変化」
- 令和5年 1月17日 メンバーを更新しました。
- 令和5年 1月6-7日 清水PLが大会長を務める第19回ファンクショナルフード学会学術集会(愛知)が開催され、澁谷研究員が口頭発表「筋疲労モデルマウスの運動機能を改善する機能性食品素材」を行いました。また、澁谷研究員が本大会で令和4年度論文賞を受賞しました。
- 令和4年 11月30日-12月2日 第45回日本分子生物学会年会(千葉)において澁谷研究員および渡辺研究員がポスター発表を行いました。
- 令和4年 11月28日 澁谷研究員の論文(Nutuarl Compounds That Enhance Motor Function in Mouse Model of Muscle Fatigue
 )がオンライン科学誌「Biomedicines」に掲載されました。
)がオンライン科学誌「Biomedicines」に掲載されました。
- 令和4年 11月19日 日本基礎老化学会第43回シンポジウム(熊本)に清水PLおよび澁谷研究員が参加しました。
- 令和4年 8月24日 第7回NCGGサマーリサーチセミナーにおいて澁谷研究員がポスター発表を行いました。「アサイー果実による造血因子エリスロポエチン 誘導作用」
- 令和4年7月28日 第45回日本基礎老化学会大会(京都)において澁谷研究員および渡辺研究員が口頭発表を行いました。また、澁谷研究員が若手奨励賞を受賞しました。「Mitochondrial ROS in fast muscle reversibly regulates glycogen metabolism and physical activity in mice」
- 令和4年 6月19日 第22回日本抗加齢医学会大会(大阪)において澁谷研究員が口頭発表を行いました。「アサイー果実は腎臓の低酸素化を介して造血ホルモンを増加する」
- 令和4年 1月 8日 第18回ファンクショナルフード学会学術集会(東京)において澁谷研究員が口頭発表を行いました。「アサイー果実パルプ水溶液は腎低酸素誘導を介して造血因子erythropoietinを増加する」
- 令和3年 12月3日 第44回日本分子生物学会年会(横浜)において澁谷研究員および渡辺研究員がポスター発表を行いました。
- 令和3年 6月12日 第44回日本基礎老化学会大会(大府)で澁谷研究員および渡辺研究員が口頭発表を行いました。
- 令和3年 4月12日 メンバー、業績を更新しました。
- 令和3年 3月21日 日本農芸化学会21年度大会で澁谷研究員がオンライン発表を行いました。
- 令和3年 3月 6日 骨格筋研究会で清水プロジェクトリーダーおよび澁谷研究員がオンライン発表を行いました。
- 令和3年 2月 6日 第2回CIBoGリトリートにおいて渡辺研究員がオンライン発表を行いました。
- 令和3年 1月12日 業績を更新しました。
- 令和2年12月 3日 日本分子生物学会第43回年会において、清水プロジェクトリーダー、澁谷研究員、渡辺研究員の3名がオンライン発表を行いました。
- 令和2年10月26日 業績を更新しました。
- 令和2年 9月10日 業績を更新しました。
- 令和2年 8月28日 第5回NCGGサマーリサーチセミナーにおいて澁谷研究員が優秀ポスター賞を受賞しました。「新しいウェルナー早老症モデルマウスの老化病態解析」
- 令和2年 7月15日 メンバー、業績を更新しました。
- 令和2年 5月28日 澁谷研究員が第43回日本基礎老化学会(長崎)で誌面発表しました。
- 令和2年 5月1日 英語版のHPを開設しました。こちらも合わせてご覧ください
- 令和2年 4月6日 メンバー、業績を更新しました。
- 令和元年 8月9日 第4回NCGGサマーリサーチセミナーにおいて清水プロジェクトリーダーが優秀ポスター賞を受賞しました。 「骨格筋ミトコンドリアで過剰発生した活性酸素種はグリコーゲン代謝酵素を失活させ、顕著なグリコーゲン蓄積による運動不耐となる」
- 令和元年 8月2日 HPを開設しました。
先頭へ戻る
主な研究テーマ
1. SOD2に着目したミトコンドリアストレス応答研究
ミトコンドリア内でレドックス制御の中心的な役割を担うSOD2(Mn-SOD)に着目して、臓器障害過程でのミトコンドリア機能の役割を調べてきました。Cre-loxpシステムを用いた臓器選択的なSOD2欠損マウスを独自に作出して、各々の臓器において、SOD2欠損でミトコンドリア機能が低下し、臓器障害が生じることを明らかにしてきました(図1)。特に運動器組織の骨格筋では、ATP枯渇による運動能力低下が認められ、骨組織では骨細胞ネットワーク破綻による骨量減少が明らかとなり(図2)、さらに軟骨組織では細胞外基質バランス破綻による軟骨変性が認められています(図3)。これらの病態は、高齢期に見られる加齢性変化と酷似しており、変形性関節症患者の軟骨組織では、SOD2が顕著に減少することから、臓器老化過程を再現している可能性があります。また、SOD2欠損により、代謝ネットワークの鍵酵素タンパク質の酸化失活やミトコンドリアストレス応答の過剰反応が生じることで、臓器障害を引き起こす分子機構の一端も判明しています。
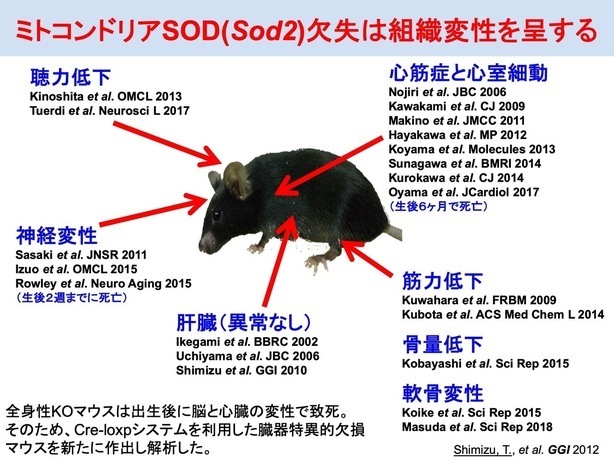
図1. SOD2欠損マウスは様々な組織変化を呈する。
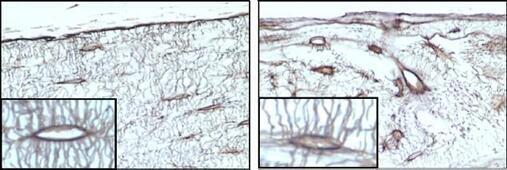
図2. 骨細胞特異的SOD2欠損マウスの大腿骨組織像。5ヶ月齢の対照マウス骨切片像(左)と同月齢の欠損マウス骨切片像(右)。骨細管構造の不整が顕著に認められる。
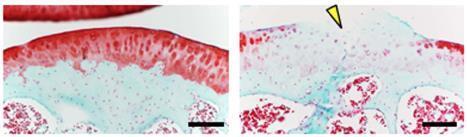
図3. 軟骨細胞特異的SOD2欠損マウスの膝軟骨組織像。12ヶ月齢の対照マウス軟骨組織切片像(左)と同月齢の欠損マウス軟骨組織切片像(右)。顕著な軟骨変性と亀裂が認められる。
2. SOD1に着目したレドックスストレス応答研究
細胞質でレドックス制御の中心的な役割を担うSOD1(CuZn-SOD)に着目して、臓器障害過程での細胞質レドックス制御の役割を調べてきました。SOD1欠損マウスの解析を通じて、加齢にともない全身の様々な臓器で加齢様の変化を示すことが明らかとなりました(図4、5)。興味深いことに、アルツハイマー病(AD)患者剖検脳に含まれるSOD1量を調べたところ、SOD1が選択的に減少していることを明らかにしました。SOD1欠損マウスとADモデルマウスを交配し、病態発症を調べたところ、Sod1遺伝子の減少に伴い、老人斑形成促進(図6)やamyloid β (Aβ) オリゴマーの増加に加え、記憶・学習能の低下が認められました。SOD1の減少による脳内でのレドックス制御不全がアルツハイマー病発症の要因になりうることを示唆しました。また最近、組織内で細胞老化マーカーの亢進も認められ、新しい老化促進モデルマウスとして注目されています。
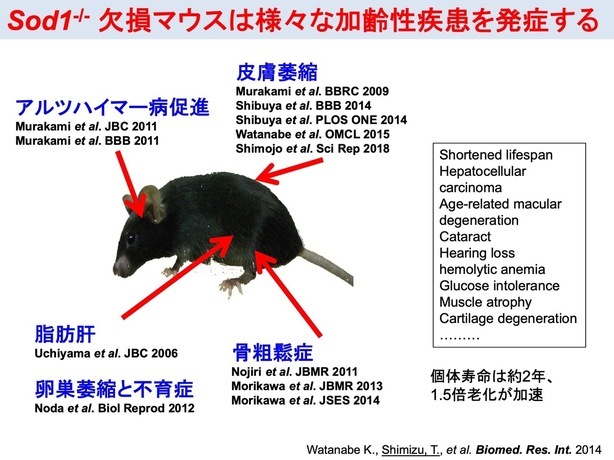
図4. SOD1欠損マウスは様々な加齢性疾患を呈する。
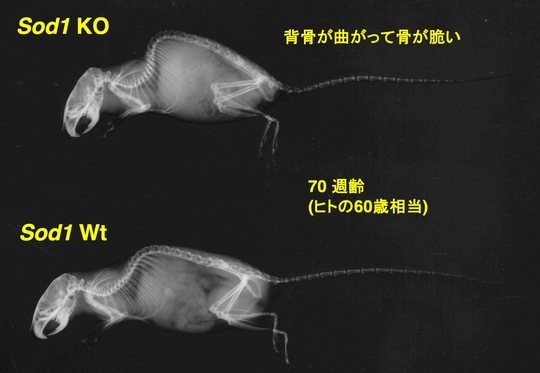
図5. SOD1欠損マウスは背骨の湾曲を伴う骨粗鬆症を呈する。
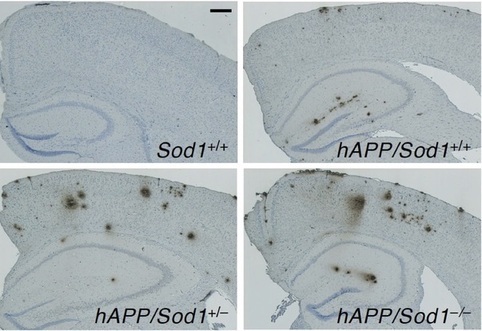
図6. SOD1量が減少すると ADモデルマウス脳は老人斑形成が促進する。
3. 機能性食品の臓器老化制御研究
1と2の老化モデルマウスは、明確な臓器老化を示すため、薬剤や食品成分の臓器老化に対する保護作用を個体レベルで調べることが可能です。さらに、酸化障害やそれに付随した分子機構に対する作用を調べることで、物質の作用メカニズムを明らかにすることもできる。高麗人参成分であるシリンガレシノールは、FoxO3a-MMP-2軸を調節することで、Sod1欠損マウスの皮膚萎縮を正常化しました(図7)。またリンゴプロシアニジンは、ミトコンドリア新生作用とプロテオグリカン産生作用で、軟骨変性を緩和しました(図8)。食品因子の新しい機能性を明らかにする研究にも取り組んでいます。
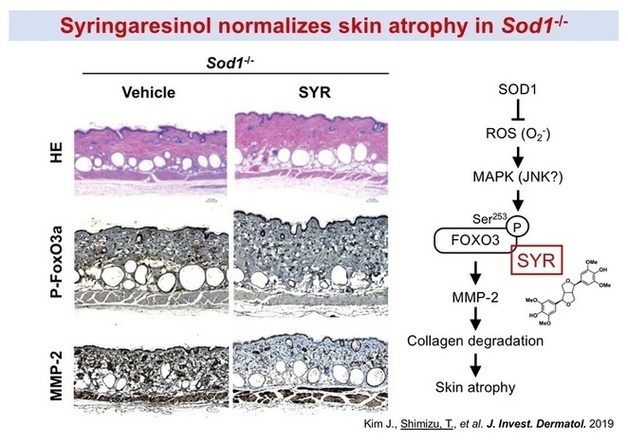
図7. 高麗人参成分のsyringaresinolは、FoxO3a-MMP-2 axisを調節することで、SOD1欠損マウスの皮膚萎縮を正常化する。
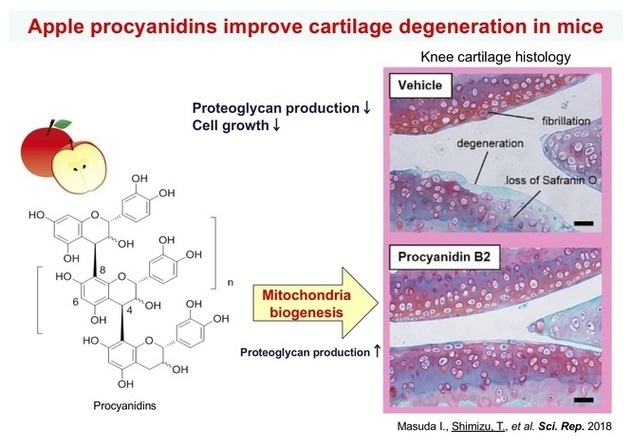
図8. りんごプロシアニジンはミトコンドリア新生作用とプロテオグリカン産生作用で、軟骨特異的SOD2欠損マウスの軟骨変性を改善する。
先頭へ戻る
研究スタッフ
| プロジェクトリーダー |
清水 孝彦 |
| 研究員 |
澁谷 修一 |
| 渡辺 憲史 |
| 研究補助員 |
山本 利奈
|
| 佐藤 穂佳 |
|
客員研究員
|
嶋本 顕 |
| 野尻 英俊 |
| 村上 一馬 |
| 竹下 淳 |
先頭へ戻る
研究業績
2009年〜、117報 (英文) *印はcorrespondence authorを示す
2023, 2022, 2021, 2020, 2019, 2018, 2017, 2016, 2015, 2014, 2013, 2012, 2011, 2010, 2009
2023年
- Shiraki, A., Oyama, J., Shimizu, T., Node, K. Linagliptin exacerbates heart failure due to energy deficiency via downregulation of glucose utilization and absorption in a mouse model. Eur J Pharmacol 948, 175673 (2023).
- 清水孝彦. 老化遺伝子とアンチエイジング.第4版アンチエイジング医学の基礎と臨床、編集:山田秀和、日本抗加齢医学会. 54-56 (2023).
- 渡辺憲史, 澁谷修一, 清水孝彦. マウス胎仔線維芽細胞の樹立.組織培養の技術 第4版、編集:日本組織培養学会編、朝倉書店、pp110-115、2023年 7月1日.
- 澁谷修一,渡辺憲史,桜庭大樹,阿部卓哉,清水孝彦. 筋疲労モデルマウスを用いた運動機能改善物質の探索.Functional Food Research,(19)45-49,2023
- 清水孝彦. 早老症モデルを用いた食品素材の機能性解析.Functional Food Research,(19)5-9,2023
- Taniwa, K., Murakami, K., Sakaguchi, Y., Izuo, N., Hanaki, M., Sampa, N., Kume, T., Shimizu, T., and Irie, K. Detection of dietary chalcone and flavonoid metabolites in mice using UPLC–MS/MS and their modulatory effects on amyloid β aggregation. J Agric Food Chem,2023 Oct4;71(39):14289-14299.doi:10.1021/acs.jafc.3c02598.
- Izuo, N., Watanabe, N., Noda, Y., Saito, T., Saido, T.C., Yokote, K., Hotta, H., Shimizu, T. Insulin resistance induces earlier initiation of cognitive dysfunction mediated by cholinergic deregulation in a mouse model of Alzheimer’s disease. Aging Cell,2023 Nov;22(11):e13994 doi:10.1111/acel.13994.Epub2023 oct11.
- 清水孝彦. アンチエイジング研究の基礎. J Mamm Ova Res, 40(2)27-33,2023
- 澁谷修一*、坂本一晃、渡辺憲史、野尻英俊、清水孝彦. 骨格筋特異的SOD2欠損はミトコンドリア機能不全に伴う運動不耐を引き起こす.基礎老化研究誌. 47(1), 32-34 (2023). 1月号
2022年
- Shuichi, S., Watanabe, K., Sakuraba, D., Abe, T., and Shimizu, T.* Natural compounds that enhance the motor function in a mouse model of muscle fatigue. Biomedicines. 10,3073(2022).
- Maki, T., Sawahata, M., Akutsu, I., Amaike, S., Hiramatsu, G., Uta, D., Izuo, N., Shimizu, T., Irie, K., Kume, T.* APP knock-in mice produce E22P-Aβ exhibiting an Alzheimer’s disease-like phenotype with dysregulation of hypoxia-3 inducible factor expression. Int J. Mol. Sci. 23(21), 13259 (2022).
- Murakami, K.*, Sakaguchi, Y., Taniwa, K., Izuo, N., Hanaki, M., Kawase, T., Hirose, K., Nagao, C., Mizoguchi, K., Shimizu, T., Irie, K.* Lysine-targeting inhibition of amyloid β oligomerization by a green perilla-derived metastable chalcone in vitro and in vivo. RSC Chem. Biol. 3, 1380 (2022).
- 清水孝彦*、澁谷修一、渡辺憲史. 酸化ストレスと運動器老化 特集:老化はなぜ進むのか? BIO Clinica(バイオクリニカ). 37(14),1287-1292(2022).
- 清水孝彦*. 第1章「老化」の不思議を科学してみると?.『眠れなくなるほど面白い 図解 老化=エイジングの話』、編集:長岡 功、日本文芸社. 2022年12月10日.
- 清水孝彦*. 加齢脳とストレス応答異常.基礎講座『エイジング・サイエンスと脳』老年精神医学雑誌. 33(9) 947-955 (2022). 9月号
- 澁谷修一,渡辺憲史,Mario Jose Villegas Yata,清水孝彦*. アサイー果実パルプ水溶液は腎低酸素誘導を介して造血因子エリスロポエチンを増加させる. Functional Food Research, 18, 65-69 (2022).
- Shiraki, A.*, Jun-ichi Oyama, J., Shimizu, T., Nakashima, T., Yokota, T., Node, K. Empagliflozin improves cardiac mitochondrial function and survival through energy regulation in a murine model of heart failure. Eur J Pharmacol. 931, 175194(2022).
- Okamoto, N., Sato, Y., Kawagoe, Y., Shimizu, T., Kawamura, K*. Short-term resveratrol treatment restored the quality of oocytes in aging mice. Aging 14(14), 5628-5640(2022).
- 清水孝彦*. SODによる骨格筋恒常性維持機構. 体力科学. 71(1) 118 (2022).
- 清水孝彦*, 渡辺憲史, 澁谷修一.酸化ストレスと骨格筋老化. 実験医学. 40(2) 78-85 (2022).
2021年
- Zhuang, A., Yang, C., Liu, Y., Tan, Y., Bond, S.T., Walker, S., Sikora, T., Laskowski, A., Sharma, A., de Haan, J.B., Meikle, P.J., Shimizu, T., Coughlan, M.T., Calkin, A.C., Drew, B.G.*. SOD2 in skeletal muscle: New insights from an inducible deletion model. Redox Biology 47, 102135 (2021).
- 渡辺憲史, 澁谷修一, 清水孝彦*. ミトコンドリアストレスと臓器障害. ミトコンドリアダイナミクス.エヌ・ティー・エス. pp.307-317 (2021).
- 清水孝彦*. 老化ストレス応答研究. 医学のあゆみ 279, 364-369 (2021).
- 清水孝彦*. 老化制御研究におけるファンクショナルフードの役割. Functional Food Research, 17, 135-141 (2021).
- Fulton,R.E., Pearson-Smith, J.N., Huynh, C.Q., Fabisiak, T., Liang, L., Aivazidis, S., High, B.A., Buscaglia, G., Corrigan, T., Valdez, R., Danis, E., Shimizu, T., and Patel, M.N.*. Neuron-specific mitochondrial oxidative stress results in epilepsy, glucose dysregulation and a striking astrocyte response. Neurobiol. Dis. 158,105470(105470(2021).
- Shibuya, S., Watanabe, K., Ozawa, Y., Shimizu, T.*. Xanthine oxidoreductase-mediated superoxide production is not involved in the age-related pathologies of Sod1-deficient mice. Int J. Mol. Sci. 22(7), 3542 (2021).
- Watanabe, K., Shibuya, S., Ozawa, Y., Toda, T., Shimizu, T.*. Pathological relationship between intracellular superoxide metabolism and p53 signaling in mice. Int J. Mol. Sci.22(7), 3548 (2021).
- 泉尾 直孝*, 清水孝彦, 村上 一馬, 入江 一浩. 毒性配座アミロイドbに着目した新規アルツハイマー病モデルマウスの開発 YAKUGAKU ZASSHI. 141(6) 843-849 (2021).
2020年
- 清水孝彦*. マトリックスメタロプロテアーゼ(MMP)と組織老化.(特集:SASPから紐解く老化と老化関連疾患) 老年内科. 2(6) 638-644 (2020).
- Watanabe, N., Noda, Y., Iimura, K., Shimizu, T., Hotta, H.*. Cerebral artery dilation during transient ischemia is impaired by mechanical barrier of amyloid β deposition around cerebral artery in Alzheimer’s disease model mice. J. Physiol. Sci. 70, 57 (2020).
- Sharma, S., Bhattarai, S., Ara, H., Sun G., St. Clair, D.K., Bhuiyan, S., Kevil, C., Watts, M.N., Dominic, P., Shimizu, T., McCarthy, K.J., Sun, H., Panchatcharam, M.*. SOD2 deficiency in cardiomyocytes defines defective mitochondrial bioenergetics as a cause of lethal dilated cardiomyopathy. Redox Biology 37, 101740, (2020).
- Obata,Y., Murakami,K.,* Kawase,T., Hirose,K., Izuo,N., Shimizu,T. and Irie,K.* Detection of Amyloid β Oligomers with RNA Aptamers in AppNL‑G‑F/NL‑G‑F Mice: A Model of Arctic Alzheimer’s Disease. ACS Omega 2020, 5, 21531−21537 (2020).
- 清水孝彦*. 臓器老化を標的にした食品素材の機能性解析. Functional Food Research. 16, 21-27 (2020).
- Teratani, T., Tomita, K.*, Toma-Fukai, S., Nakamura, Y., Itoh, T., Shimizu, H., Shiraishi, Y., Sugihara, N., Higashiyama, M., Shimizu, T., Inoue, I., Takenaka, Y., Hokari, R., Adachi, T., Shimizu, T., Miura, S. Kanai, T. Redox-dependent PPARg/Tnpo1 complex formation enhances PPARg nuclear localization and signaling. Free Radic. Biol. Med. 156, 45-56 (2020).
- 清水孝彦*. 加齢と骨代謝(連載:老化研究の進歩). 医学のあゆみ. 273(7) 600-606 (2020).
- Murakami, K.*, Obata, Y., Sekikawa, A., Ueda, H., Izuo, N., Awano, T., Takabe, K., Shimizu, T., Irie, K.* An RNA aptamer with potent affinity for a toxic dimer of amyloid β42 has potential utility for histochemical studies of Alzheimer’s disease. J. Biol. Chem. 295, 4870-4880 (2020).
- Shibuya, S., Toda, T., Ozawa, Y., Yata, M.J.V., Shimizu, T.* Acai extract transiently upregulates erythropoietin by inducing a renal hypoxic condition in mice. Nutrients, 12(2), 533 (2020).
- Yagi-Yaguchi, Y., Kojima, T., Higa, K., Dogru, M.*, Ibrahim, O., Shimizu, T., Tsubota, K. Shimazaki, J. The effects of 3% diquafosol sodium eye drops on tear functions and ocular surface of the Cu, Zn-superoxide dismutase-1 (Sod1) knock out mice treated with antiglaucoma eye medications. Diagnostics 10, 20 (2020).
- Sagi, H., Shibuya, S., Kato, T., Nakanishi, Y., Tsuboi, A., Moriya, S., Ohno, H., Miyamoto, H., Kodama, H.*, Shimizu, T. SOD1 deficiency alters gastrointestinal microbiota and metabolites in mice. Exp. Gerontol. 130, 110795 (2020).
2019年
- Sakamoto, K., Furuichi, Y., Yamamoto, M., Takahashi, M., Akimoto, Y., Ishikawa, T., Shimizu, T., Fujimoto, M., Takada-Watanabe, A., Hayashi, A., Mita, Y., Manabe, Y., Fujii, N., Ishibashi, R., Maezawa, Y., Betsholtz, C., Yokote, K., Takemoto, M*. R3h domain containing-like regulates satellite cell proliferation and differentiation. EMBO Rep., 20, e47957 (2019).
- Kim, J., Funayama, S., Izuo, N., Shimizu, T.* Dietary supplementation of a high-temperature-processed green tea extract attenuates cognitive impairment in PS2 and Tg2576 mice. Biosci. Biotechnol. Biochem. 83(12), 2364-2371 (2019).
- Uchitomi, R., Hatazawa, Y., Senoo, N., Yoshioka, K., Fujita, M., Shimizu, T., Miura, S., Ono, Y., Kamei, Y.* Metabolomic analysis of skeletal muscle in aged mice. Sci. Rep. 9, 10425, DOI: 10.1038/s41598-019-46929-8 (2019).
- Dogru, M.*, Shinzawa, M., Kojima, T., Shimizu, T., Tsubota, K. Age related conjunctival P2Y2 receptor alterations in the Cu, Zn-superoxide dismutase-1 (Sod1)–knockout dry eye model mice. Eye & Contact Lens 45(6), 405-409 (2019).
- Andergassen, D., Muckenhuber, M., Bammer, C.P., Kulinski, M.T., Theussl, H-C., Shimizu, T., Penninger, M.J., Pauler M.F., and Hudson, J.Q.* Deletion of the Airn lncRNA gene shows that RNA mediated silencing of distant imprinted genes does not require any genetic elements within the gene. PLoS Genet. 15(7), e1008268 (2019).
- Shibuya, S., Watanabe, K., Tsuji, G., Ichihashi, M., Shimizu, T.* Platinum and palladium nanoparticles-containing mixture, PAPLAL, does not induce palladium allergy. Exp. Dermatol. 28(9), 1025-1028 (2019).
- Izuo, N., Murakami, K., Fujihara, Y., Maeda, M., Saito, T., Saido, T., Irie, Y., Shimizu, T.* An App knock-in mouse inducing the formation of a toxic conformer of Aβ as a model for evaluating only oligomer-induced cognitive decline in Alzheimer’s disease. Biochem. Biophys. Res. Commun., 515(3), 462-467 (2019).
- Ozawa, Y., Watanabe, K., Toda, T., Shibuya, S., Okumura, N., Okamoto, N., Sato, Y., Kawashima, I., Kawamura, K., Shimizu, T.* Heterosis extends the reproductive ability in aged female mice. Biol Reprod 100(4), 1082-1089 (2019).
- Kim, J., Toda, T., Watanabe, K., Shibuya, S., Ozawa, Y., Izuo, N., Cho, S., Seo, D.B., Yokote, K., Shimizu, T.* Syringaresinol reverses age-related skin atrophy by suppressing FoxO3a-mediated matrix metalloproteinase–2 activation in copper/zinc superoxide dismutase–deficient mice. J. Investig. Dermatol., 139(3), 648-655 (2019).
2018年
- Okumura, N., Toda, T., Ozawa, Y., Watanabe, K., Ikuta, T., Tatefuji, T., Hashimoto, K., Shimizu, T.* Royal jelly delays motor functional impairment during aging in genetically heterogeneous male mice. Nutrients, 10(9), E1191 (2018).
- Shimojo, Y., Ozawa, Y., Toda, T., Igami, K., Shimizu, T.* Probiotic Lactobacillus paracasei A221 improves functionality and bioavailability of kaempferol-glucoside in kale by its glucosidase activity. Sci. Rep. 8, 9239, DOI: 10.1038/s41598-018-27532-9 (2018).
- Masuda, I., Koike, M., Nakashima, S., Mizutani, Y., Ozawa, Y., Watanabe, K., Sawada, Y., Sugiyama, H., Sugimoto, A., Nojiri, H., Sashihara, K., Yokote, K., Shimizu, T.* Apple procyanidins promote mitochondrial biogenesis and proteoglycan biosynthesis in chondrocytes. Sci. Rep. 8, 7229, DOI:10.1038/s41598-018-25348-1 (2018).
- Ikeda, K., Simsek, C., Kojima, T., Higa, K., Kawashima, M., Dogru, M.*, Shimizu, T., Tsubota, K., Shimazaki, J. The effects of 3% diquafosol sodium eye drop application on meibomian gland and ocular surface alterations in the Cu, Zn-superoxide dismutase-1 (Sod1)-knockout mice. Graefes Arch. Clin. Exp. Ophthalmol. 256(4), 739-759 (2018)
- Kojima, T., Simsek, C., Igarashi, A., Aoki, K., Higa, K., Shimizu, T., Dogru, M.*, Tsubota, K., Shimazaki, J. The role of 2% rebamipide eye drops related to conjunctival differentiation in the superoxide dismutase-1 (Sod1) knockout mice. Invest. Ophthalmol. Vis. Sci. 59(3), 1675-1681 (2018).
- Morikawa, D., Nojiri, H.*, Itoigawa, Y., Ozawa, Y., Kaneko, K., Shimizu, T. Antioxidant treatment with vitamin C attenuated rotator cuff degeneration caused by oxidative stress in Sod1 deficient mice. J Shoulder Elbow Surg Open Access 2(1), 91-96 (2018).
- Hatazawa, Y., Ono, Y., Hirose, Y., Kanai, S. Fujii, N., Machida, S., Nishino, I., Shimizu, T., Okano, M., Kamei*, Y., Ogawa, Y*. Reduced Dnmt3a increases Gdf5 expression with suppressed satellite cell differentiation and impaired skeletal muscle regeneration. FASEB J 32(3), 1452-1467 (2018).
- Ho, GT.*, Aird, R., Liu, B., Kennedy, N., Dorward, D., Noble, C., Shimizu, T., Morton, N., Rossi, A., Sartor, RB., Iredale, Satsangi, J. MDR1-deficiency impairs mitochondrial homeostasis and promotes intestinal inflammation. Mucosal Immunol. 11(1), 120-130 (2018).
2017年
- Izuo, N., Kasahara, C., Murakami, K., Kume, T., Maeda, M., Irie, Y., Yokote, K., Shimizu, T.* A Toxic Conformer of Aβ42 with a Turn at 22-23 is a Novel Therapeutic Target for Alzheimer’s Disease. Sci. Rep. 7, 11811, DOI: 10.1038/s41598-017-11671-6 (2017).
- Shibuya, S., Sakaguchi, I., Ito, S., Kato, E., Watanabe, K., Izuo, N., Shimizu, T.* Topical application of trisodiumL-ascorbyl 2-phosphate 6-palmitate 2-phosphate actively supplies ascorbate into skin cells in an ascorbate transporter-independent manner. Nutrients, 9(7), E645 (2017).
- Tuerdi, A. Kinoshita, M., Kamogashira, T., Fujimoto, C. Iwasaki, S., Shimizu, T., Yamasoba, T.* Manganese superoxide dismutase influences the extent of noise-induced hearing loss in mice. Neurosci. Lett. 642, 123-128 (2017).
- Juewon Kim, Si Young Cho, Su Hwan Kim, Donghyun Cho, Sunmi Kim, Chan-Woong Park, Shimizu, T., Jae Youl Cho, Dae Bang Seo*, Song Seok Shin*. Effects of Korean ginseng berry on skin anti-pigmentation and anti-aging via FoxO3a activation. J. Ginseng Res. 41(3), 277-283 (2017).
- Oyama, J.*, Shirakihara, A., Nishikido, T., Maeda, T., Komoda, H., Shimizu, T., Makino, N., Node, K. EGCG, a green tea catechin, attenuates the progression of heart failure induced by the heart/muscle-specific deletion of MnSOD in mice. J Cardiol. 69(2), 417-427 (2017).
2016年
- Murakami, K., Tokuda, M., Suzuki, T., Irie, Y., Hanaki, M., Izuo, N., Monobe, Y., Akagi, K., Ishii, R., Tatebe, H., Tokuda, T., Maeda, M., Kume, T., Shimizu, T., Irie, K.*. Monoclonal antibody with conformational specificity for a toxic conformer of amyloid b42 and its application toward the Alzheimer's disease diagnosis. Sci. Rep. 6, 29038 (2016).
2015年
- Kojima, T., Dogru, M.*, Ibrahim, O. M., Wakamatsu, T. H., Ito, M., Igarashi, A., Inaba, T., Shimizu, T., Shirasawa, T. Shimazaki, J., Tsubota, K. The effects of 2% rebapimide ophthalmic solution on the tear functions and ocular surface of the superoxide dismutase-1 (Sod1) knockout mice. Invest. Ophthalmol. Vis. Sci. 54(12), 7793-7802 (2015).
- Shibuya, S., Watanabe, K., Yokote, K., and Shimizu, T.* Platinum and palladium nanoparticles regulate the redox balance and protect against age-related skin changes in mice. Textbook of Aging Skin, Springer-Verlag Berlin Heidelberg M.A. Farage et al. (eds.), DOI 10.1007/978-3-642-27814-3_120-1, pp1-11 (2015). ISBN: 978-3-642-27814-3 (Online)
- Koike, M., Nojiri, H., Ozawa, Y., Watanabe, K., Muramatsu, Y., Kaneko, H., Morikawa, D., Kobayashi, K., Saita, Y., Sasho, T., Shirasawa, T., Yokote, K., Kaneko, K., Shimizu, T.* Mechanical overloading causes mitochondrial superoxide and SOD2 imbalance in chondrocytes resulting in cartilage degeneration. Sci. Rep. 5, 11722 DOI: 10.1038/srep11722 (2015).
- Kobayashi, K., Nojiri, H., Saita, Y., Morikawa, D., Ozawa, Y., Watanabe, K., Koike, M., Asou, Y., Shirasawa, T., Yokote, K., Kaneko, K., Shimizu, T.* Mitochondrial superoxide in osteocyte perturbs canalicular networks in the setting of age-related osteoporosis. Sci. Rep. 5, 9148 DOI: 10.1038/srep09148 (2015).
- Munetomo, A., Hojo, Y., Higo, S., Kato, A., Yoshida, K., Shirasawa, T., Shimizu, T., Kimoto, T., and Kawato, S.* Aging-induced changes in sex-steroidogenic enzymes and sex-steroid receptors in cortex, hypothalamus and cerebellum. J Physiol Sci 65(3), 253-263 (2015).
- Izuo, N., Nojiri, H., Uchiyama, S., Noda, Y., Kawakami, S., Kojima, S., Sasaki, T., Shirasawa, T., Shimizu, T.* Brain-specific superoxide dismutase 2 deficiency causes perinatal death with spongiform encephalopathy in mice. Oxid. Med. Cell. Longev. 2015, 238914, 10 pages (2015).
- Rowley, S., Liang, LP., Fulton, R., Shimizu, T., Day, B., Patel, M.* Mitochondrial respiration deficits driven by reactive oxygen species in experimental temporal lobe epilepsy. Neurobiol. Dis., 75, 151-158 (2015).
- Watanabe, K., Shibuya, S., Ozawa, Y., Izuo, N., Shimizu, T.* Resveratrol derivative-rich melinjo seed extract attenuates skin atrophy in Sod1-deficient mice. Oxid. Med. Cell. Longev. 2015, 391075, 8 pages (2015).
2014年
- Shimamoto, A.*, Kagawa, H., Zensho, K., Sera, Y., Kazuki, Y., Osaki, M., Mitsuo Oshimura, Ishigaki, Y., Hamasaki, K., Kodama, Y., Yuasa, S., Fukuda, K., Hirashima, K., Seimiy, H., Koyama, H., Shimizu, T., Takemoto, M., Yokote, K., Goto, M., and Tahara, H.* Reprogramming Suppresses Premature Senescence Phenotypes of Werner Syndrome Cells in Long-Term Culture. PLoS One 9(11), e112900 (2014).
- Sunagawa, T., Masuda, I., and Shimizu, T.* Anti-aging effects of apple procyanidins. Proanthocyanidins: Food Sources, Antioxidant Properties and Health Benefits Chapter 6, pp139-159 (2014). November (Nova Science Publishers).
- Shibuya, S., Ozawa, Y., Watanabe, K., Izuo, N., Yokote, K., and Shimizu, T.* Palladium and platinum nanoparticles attenuate aging-like skin atrophy via antioxidant activity in mice. PLoS One 9(10), e109288 (2014).
- Watanabe, K., Shibuya, S., Ozawa, Y., Nojiri, H., Izuo, N., Yokote, K., and Shimizu, T.* Superoxide dismutase 1 loss disturbs intracellular redox signaling, resulting in global age-related pathological changes. BioMed Res. Int. 2014, 140165, 10 pages (2014).
- Ibrahim, O.M., Dogru*, M., Matsumoto, Y., Igarashi, A., Kojima, Wakamatsu, T.H.F., Inaba, T., Shimizu, T., Shimazaki, J., Tsubota, K. Oxidative stress induced age dependent meibomian gland dysfunction in Cu, Zn-superoxide dismutase-1 (Sod1) knockout mice. PLoS One 9(7), e99328 (2014).
- Miyazaki, Y., Kaneko, K., Mizushige, T., Kanamoto, R., Yoshikawa, M., Shimizu, T., and Ohinata, K.* Orally administered a δ opioid agonist peptide rubiscolin-6 stimulates food intake in aged mice with ghrelin resistance. Mol. Nutr. Food Res. 58(10), 2046-2052 (2014).
- Kondo, Y., Masutomi, H., Noda, Y., Ozawa, Y., Takahashi, K., Handa, S., Maruyama, N., Shimizu, T., and Ishigami, A.* Senescence marker protein-30/Superoxide dismutase 1 double knockout mice exhibit increased oxidative stress and hepatic steatosis. FEBS Open Bio. 4, 522-532 (2014).
- Kurokawa, S.*, Niwano, S., Niwano, H., Murakami, M., Ishikawa, S., Masaki, Y., Tamaki, H., Toda, T., Noda, Y., Shimizu, T., Izumi, T., Ako, J. Cardiomyocyte-derived Mitochondrial Superoxide Causes Myocardial Electrical Remodeling by Down-regulating Potassium Channels and Related Molecules.. Cir. J. 78(8), 1950-1959 (2014).
- Murakami, K.*, Irie, K., and Shimizu, T.* Potential role of vitamin C in the prevention of Alzheimer’s disease. Diet and Nutrition Dementia and Cognitive Decline Chapter 61, pp663-668 (2014). (Editor, Preedy, V.R., Elsevier Publishers).
- Kubota, R., Imamura, S., Shimizu, T., Asayama, S., Kawakami, H.* Synthesis of water-soluble dinuclear manganese porphyrin with multiple antioxidative activities. ACS Med. Chem. Letters. 5(6), 639-643 (2014).
- Shibuya, S., Ozawa, Y., Toda, T., Watanabe, K., Tometsuka, C., Ogura, T., Koyama, Y., and Shimizu, T.* Collagen peptides and vitamin C additively attenuate age-related skin atrophy in Sod1-deficient mice. Biosci. Biotechnol. Biochem. 78(7), 1212-1220 (2014).
- Sunagawa, T.*, Shimizu, T., Matsumoto, A., Tagashira, M., Kanda, T., Shirasawa, T., Nakaya, H. Electrophysiological alterations in the heart of heart/muscle-specific Mn-superoxide dismutasedeficient mice. BioMed. Res. Int. 2014, 704291, 12 pages (2014).
- Morikawa, D., Itoigawa, Y., Nojiri, H., Sano, H., Itoi, E., Saijo, Y., Kaneko, K., Shimizu, T.* Contribution of oxidative stress to the degeneration of rotator cuff entheses. J Shoulder Elbow Surg. 23(5), 628-635 (2014).
- Kojima, T., Dogru, M.*, Ibrahim, O. M., Nagata, T., Higa, K., Shimizu, T., Shirasawa, T., Satake, Y., Shimazaki, S. Tsubota, T., Shimazaki, J. The effects of 3% diquafosol sodium application on the tear functions and ocular surface of the Cu,Zn-superoxide dismutase-1 (Sod1)–knockout mice. Mol Vision 20, 929-938 (2014).
- Shibuya, S., Nojiri, H., Morikawa, D., Koyama, H., and Shimizu, T.* Protective effects of vitamin C on age-related bone and skin phenotypes caused by intracellular reactive oxygen species. Aging: Oxidative Stress and Dietary Antioxidants Chapter 14, pp137-144 (2014). (Editor, Preedy, V.R., Elsevier Publishers).
- Shimizu, T.*, Nojiri, H., and Shirasawa, T. Tissue-specifc deletion of Mn-SOD in mice. Systems Biology of Free Radicals and Antioxidants (Editor, Laher, I., Springer Publishers). Chapter 22, 475-487 (2014). Publication Date: April 30, 2014 | ISBN-10: 3642300170 | ISBN-13: 978-3642300172
2013年
- Ohguchi, T.*, Kojima, T., Ibrahim, O. M., Nagata, T., Shimizu, T., Shirasawa, T., Kawakita, T., Satake, Y., Tsubota, T., Shimazaki, J., Ishida, S. The effects of 2% rebapimide ophthalmic solution on the tear functions and ocular surface of the superoxide dismutase-1 (Sod1) knockout mice. Invest. Ophthalmol. Vis. Sci. (Investigative Ophthalmology & Visual Science) 54(12), 7793-7802 (2013)
- Kinoshita, M., Sakamoto, T., Kashio, A., Shimizu, T., and Yamasoba, T.* Age-related hearing loss in Mn-SOD heterozygous knockout mice. Oxid. Med. Cell. Longev. 2013, 325702, 13pages (2013).
- Izuo, N., Murakami, K., Sato, M., Iwasaki, M., Izumi, Y., Shimizu, T., Akaike, A., Irie, K.*, and Kume, T.* Non-toxic conformer of amyloid β may suppress amyloid β-induced toxicity in rat primary neurons: implications for a novel therapeutic strategy for Alzheimer’s disease. Biochem. Biophys. Res. Commun. 438(1), 1-5 (2013).
- Watanabe, K., Shibuya, S., Koyama, H., Ozawa, Y., Toda, T., Yokote, K., and Shimizu, T.* Sod1 loss induces intrinsic superoxide accumulation leading to p53-mediated growth arrest and apoptosis. Int. J. Mol. Sci. 14(6), 10998-11010 (2013).
- Morikawa, D., Nojiri, H., Saita, Y., Kobayashi, K., Watanabe, K., Ozawa, Y., Koike, M., Asou, Y., Takaku, T., Kaneko, K., Shimizu, T.* Cytoplasmic reactive oxygen species and SOD1 regulate bone mass during mechanical unloading. J. Bone Miner. Res. 28(11), 2368-2380 (2013).
- Koyama, H., Nojiri, H., Kawakami, S., Sunagawa, T., Shirasawa, T., Shimizu, T.* Antioxidants improve the phenotypes of dilated cardiomyopathy and muscle fatigue in mitochondorial superoxide dismutase-deficinet mice. Molecules 18, 1383-1393 (2013).
2012年
- Kulic, L.*, McAfoose, J., Welt, T., Tackenberg, C., Späni, C., Wirth, F., Finder, V., Konietzko, U., Giese, M., Eckert, A., Kinoshita, N., Shimizu, T., Murakami, K., Irie, K., Rasool, S., Glabe, C., Hock, C., & Nitsch, R. M. Early accumulation of intracellular fibrillar oligomers and late congophilic amyloid angiopathy in mice overexpressing the Osaka intra-Aβ APP mutation. Transl Psychiatry 13(2), e183 (2012).
- Hayakawa, N., Asayama, S., Noda, Y., Shimizu, T., and Kawakami, S.* Pharmaceutical effect of manganese porphyrins on manganese superoxide dismutase deficient mice. Mol Pharm 9, 2956-2959 (2012).
- Sunagawa, T., Watanabe, K., Ozawa, Y., Nakashima, S., Kanda, T., Tagashira, M., Sami, M., Kaneko, T., Tahara, T., Nakaya, H., Shirasawa, T., Shimizu, T.* Apple polyphenols regulate mitochondrial superoxide generation and extend survival in a mouse model of dailated cardiomyopathy. Int J Life Sci Med Res, 2, 46-51 (2012).
- Fujita, H.*, Fujishima, H., Takahashi, K., Sato, T., Shimizu, T., Morii, T., Shimizu, T., Shirasawa, T., Qi, Z., Breyer, M., Harris, C., Yamada, Y. and Takahashi, T.* SOD1, but not SOD3, deficiency accelerates diabetic renal injury in C57BL/6-Ins2Akita diabetic mice. Metabolism 61, 1714-1724 (2012).
- Lustgarten, M., Bhattacharya, A., Muller, F., Jang, Y., Shimizu, T., Shirasawa, T., Richardson, A. and Van Remmen, H.*. Complex I generated, mitochondrial matrix-directed superoxide is released from the mitochondria through voltage dependent anion channels. Biochem Biophys Res Commun 422, 515-521 (2012).
- Murakami, K., Murata, N., Noda, Y., Irie, K., Shirasawa, T. & Shimizu, T.* Stimulation of the amyloidogenic pathway by cytoplasmic superoxide radicals in an Alzheimer’s disease mouse model. Biosci Biotechnol Biochem 76, 1098-1103 (2012).
- Takahashi, M.*, Shimizu, T. & Shirasawa, T. Reversal of slow growth and heartbeat through the restoration of mitochondrial function in clk-1-deficient mouse embryos by exogenous administration of coenzyme Q10. Exp Gerontol 47, 425-431 (2012).
- Murakami, K., & Shimizu, T.* Cytoplasmic superoxide radical: a possible contributing factor to intracellular Ab oligomerization in Alzheimer’s disease. Commun. Integ. Biol. 5, 255-258 (2012).
- Kojima, T., Wakamatsu, H. T., Dogru, M.*, Ogawa, Y., Igarashi, A., Ibrahim, O., Inaba, T., Shimizu, T., Noda, S., Obata, H., Nakamura, S., Wakamatsu, A., Shirasawa, T., Shimazaki, J., Negishi, K., Tsubota, K. Age-related dysfunction of the lacrimal gland and oxidative stress: Evidence from the Cu,Zn-superoxide dismutase-1 (Sod1) knockout mice. Am J Pathol 180, 1879-1896 (2012).
- Takahashi, M.*, Ogawara, M., Shimizu, T. & Shirasawa, T. Restoration of the behavioral rates and lifespan in clk-1 mutant nematodes in response to exogenous coenzyme Q10. Exp Gerontol 47, 276-279 (2012).
- Ogawa, K.*, Kim, H., Shimizu, T., Abe, S., Shiga, Y., Calderwood, S. Plasma heat shock protein 72 as a biomarker of sarcopenia in elderly people. Cell Stress & Chaperones 17, 349-359 (2012).
- Noda, Y., Ota, K., Shirasawa, T. & Shimizu, T.* CuZn-SOD insufficiency impairs progesterone secretion and fertility in female mice. Biol Reprod 86, 1-8 (2012).
- Miura, G., Kato, K., Shimizu, T., Shiga, D., Shirasawa, T.* Heme oxygenase1 is constitutively up-regulated in top climbers. Biochem Biophys Res Commun 417, 104-108 (2012).
- Shibuya, S., Kinoshita, K., Shimizu, T.* Protective effects of vitamin C derivatives on skin atrophy caused by Sod1 deficiency. Handbook of Diet, Nutrition and the Skin Chapter 21, pp350-364 (2012). (Editor, Preedy, V.R., Wageningen Academic Publishers).
2011年
- Murakami, K., Murata, N., Noda, Y., Tahara, S., Kaneko, T., Kinoshita, N., Hatsuta, H., Murayama, S., Barnham, K., J., Irie, K., Shirasawa, T. & Shimizu, T.* SOD1 (copper/zinc superoxide dismutase) deficiency drives amyloid b oligomerization and memory loss in a mouse model of Alzheimer’s disease. J. Biol. Chem. 286, 44557-44568 (2011).
- Nojiri, H., Saita, Y., Morikawa, D., Kobayashi, K., Tsuda, C., Miyazaki, T., Saito, M., Marumo, K., Yonezawa, I., Kaneko, K., Shirasawa, T., Shimizu, T.* Cytoplasmic superoxide causes bone fragility owing to low-turnover osteoporosis and impaired collagen cross-linking. J. Bone Miner. Res. 26, 2682-2694 (2011).
- Jones, M. K.*, Zhu, E., Sarino, E. V., Padilla, O. R., Takahashi, T., Shimizu, T., Shirasawa, T. Loss of parietal cell superoxide dismutase leads to gastric oxidative stress and increased injury susceptibility in mice. Am. J. Physiol.-Gastr. L. 301, G537-G546 (2011).
- Toda, T., Sunagawa, T., Kanda, T., Tagashira, M., & Shirasawa, T. Shimizu, T.* Apple procyanidins suppress amyloid-b protein aggregation. Biochem Res Int 2011, 784698 (2011).
- Shimizu, T.*, Baba, T., Ogawara, M., & Shirasawa, T. Lifespan and glucose metabolism in insulin receptor mutant mice. J Aging Res 2011, 315640 (2011).
- Murakami, K., Murata, N., Ozawa, Y., Kinoshita, N., Irie, K., Shirasawa, T. & Shimizu, T.* Vitamin C restores behavioral deficits and amyloid-b oligomerization without affecting plaque formation in a mouse model of Alzheimer's disease. J Alzheimers Dis 26, 7-18 (2011).
- Murakami, K., Yokoyama, S.I., Murata, N., Ozawa, Y., Irie, K., Shirasawa, T. & Shimizu, T.* Insulin receptor mutation results in insulin resistance and hyperinsulinemia but does not exacerbate Alzheimer's-like phenotypes in mice. Biochem Biophys Res Commun 409, 34-39 (2011).
- Parajuli, N., Marine, A., Simmons, S., Saba, H., Mitchell, T., Shimizu, T., Shirasawa, T. & MacMillan-Crow, L.* A. Generation and characterization of novel kidney-specific manganese superoxide dismutase knockout mouse. Free Radic Biol Med 51, 406-416 (2011).
- Toda, T., Noda, Y., Ito, G., Maeda, M. & Shimizu, T.* Presenilin-2 mutation causes early amyloid accumulation and memory impairment in a transgenic mouse model of Alzheimer's disease. J Biomed Biotechnol 2011, 617974 (2011).
- Sasaki, T.*, Shimizu, T., Koyama, T., Sakai, M., Uchiyama, S., Kawakami, S., Noda, Y., Shirasawa, T. & Kojima, S. Superoxide dismutase deficiency enhances superoxide levels in brain tissues during oxygenation and hypoxia-reoxygenation. J Neurosci Res 89, 601-610 (2011).
- Murakami, K.*, Shimizu, T. & Irie, K. Formation of the 42-mer amyloid β radical and the therapeutic role of superoxide dismutase in Alzheimer’s disease. J Amino Acid 2011, 654207 (2011). 査読有
- Sunagawa, T., Shimizu, T.*, Kanda, T., Tagashira, M., Sami, M. & Shirasawa, T.* Procyanidins from apples (Malus pumila Mill.) extend the lifespan of Caenorhabditis elegans. Planta Med 77, 122-127 (2011).
- Ogawa, K.*, Seta, R., Shimizu, T., Shinkai, S., Calderwood, S.K., Nakazato, K. & Takahashi, K. Plasma adenosine triphosphate and heat shock protein 72 concentrations after aerobic and eccentric exercise. Exerc Immunol Rev 17, 136-149 (2011).
- Makino, N.*, Maeda, T., Oyama, J.I., Sasaki, M., Higuchi, Y., Mimori, K. & Shimizu, T. Antioxidant therapy attenuates myocardial telomerase activity reduction in superoxide dismutase-deficient mice. J Mol Cell Cardiol 50, 670-677 (2011).
- Lustgarten, M.S., Jang, Y.C., Liu, Y., Qi, W., Qin, Y., Dahia, P.L., Shi, Y., Bhattacharya, A., Muller, F.L., Shimizu, T., Shirasawa, T., Richardson, A. & Van Remmen, H.* MnSOD deficiency results in elevated oxidative stress and decreased mitochondrial function but does not lead to muscle atrophy during aging. Aging Cell 10, 493-505 (2011).
- Shimizu, T.*, Shirasawa, T. Biomarkers for aging. Nihon Yakurigaku Zasshi 138, 60-63 (2011).
- Sakuramoto, H., Uchimaru, J., Naito, H., Waga, T., Sunayama, S., Shimizu, T., Kurosawa, H. & Shirasawa, T.* Dietary factors alter the oxygen affinity of hemoglobin. Juntendo Med J 57, 624-629 (2011).
2010年
- Murakami, K., Horikoshi-Sakuraba, Y., Murata, N., Noda, Y., Masuda, Y., Kinoshita, N., Hatsuta, H., Murayama, S., Shirasawa, T., Shimizu, T. & Irie, K.* Monoclonal antibody against the turn of the 42-residue amyloid β-protein at positions 22 and 23. ACS Chem Neurosci 1, 747-756 (2010).
- Shimojo, Y., Kosaka, K., Noda, Y., Shimizu, T.* & Shirasawa, T.* Effect of rosmarinic acid in motor dysfunction and life span in a mouse model of familial amyotrophic lateral sclerosis. J Neurosci Res 88, 896-904 (2010).
- Shimizu, T.*, Nojiri, H., Kawakami, S., Uchiyama, S. & Shirasawa, T. Model mice for tissue-specific deletion of the manganese superoxide dismutase (Mn-SOD) gene. Geriatr Gerontol Int 10, S70-S79 (2010).
- Murata, N., Murakami, K., Ozawa, Y., Kinoshita, N., Irie, K., Shirasawa, T. & Shimizu, T.* Silymarin attenuated the amyloid beta plaque burden and improved behavioral abnormalities in an Alzheimer's disease mouse model. Biosci Biotechnol Biochem 74, 2299-2306 (2010).
- Murakami, K., Masuda, Y., Shirasawa, T., Shimizu, T. & Irie, K.* The turn formation at positions 22 and 23 in the 42-mer amyloid β peptide: The emerging role in the pathogenesis of Alzheimer’s disease. Geriatr Gerontol Int 10, S169-S179 (2010).
- Taneike, M., Yamaguchi, O., Nakai, A., Hikoso, S., Takeda, T., Mizote, I., Oka, T., Tamai, T., Oyabu, J., Murakawa, T., Nishida, K., Shimizu, T., Hori, M., Komuro, I., Shirasawa, T., Mizushima, N. & Otsu, K.* Inhibition of autophagy in the heart induces age-related cardiomyopathy. Autophagy 6, 600-606 (2010).
- Kuwahara, H., Horie, T., Ishikawa, S., Tsuda, C., Kawakami, S., Noda, Y., Kaneko, T., Tahara, S., Tachibana, T., Okabe, M., Melki, J., Takano, R., Toda, T., Morikawa, D., Nojiri, H., Kurosawa, H., Shirasawa, T. & Shimizu, T.* Oxidative stress in skeletal muscle causes severe disturbance of exercise activity without muscle atrophy. Free Radic Biol Med 48, 1252-1262 (2010).
- Kinouchi, T.*, Matsuda, A., Kawakami, S., Shimizu, T., Shirasawa, T. & Fujii, N. Influence of oxidative stress on D-aspartyl endopeptidase activity. Chem Biodivers 7, 1398-1402 (2010).
- Shimizu, T.*, Shirasawa, T. Anti-aging research using Mn-SOD conditional knockout mice. Yakugaku Zasshi 130, 19-24 (2010).
2009年
- Murakami, K., Inagaki, J., Saito, M., Ikeda, Y., Tsuda, C., Noda, Y., Kawakami, S., Shirasawa, T. & Shimizu, T. Skin atrophy in cytoplasmic SOD-deficient mice and its complete recovery using a vitamin C derivative. Biochem Biophys Res Commun 382, 457-461 (2009).
- Masuda, Y., Uemura, S., Ohashi, R., Nakanishi, A., Takegoshi, K., Shimizu, T., Shirasawa, T. & Irie, K.* Identification of Physiological and Toxic Conformations in Ab42 Aggregates. Chembiochem 10, 287-295 (2009).
- Lustgarten, M.S., Jang, Y.C., Liu, Y., Muller, F.L., Qi, W., Steinhelper, M., Brooks, S.V., Larkin, L., Shimizu, T., Shirasawa, T., McManus, L.M., Bhattacharya, A., Richardson, A. & Van Remmen, H.* Conditional knockout of Mn-SOD targeted to type IIB skeletal muscle fibers increases oxidative stress and is sufficient to alter aerobic exercise capacity. Am J Physiol Cell Physiol 297, C1520-1532 (2009).
- Kawakami, S., Matsuda, A., Sunagawa, T., Noda, Y., Kaneko, T., Tahara, S., Hiraumi, Y., Adachi, S., Matsui, H., Ando, K., Fujita, T., Maruyama, N., Shirasawa, T. & Shimizu, T.* Antioxidant, EUK-8, prevents murine dilated cardiomyopathy. Cir J 73, 2125-2134 (2009).
- Chiba, T., Kamei, Y.*, Shimizu, T., Shirasawa, T., Katsumata, A., Shiraishi, L., Sugita, S., Ogawa, Y., Miura, S. & Ezaki, O. Overexpression of FOXO1 in skeletal muscle does not alter longevity in mice. Mech Ageing Dev 130, 420-428 (2009).
先頭へ戻る
研究員募集
現在、本プロジェクトチームでは研究員、研究補助員を募集しています。老化の分子メカニズム研究にご興味のある方はお気軽にご連絡ください。
先頭へ戻る
連絡先

清水 孝彦
〒474-8511
愛知県大府市森岡町7-430
国立研究開発法人 国立長寿医療研究センター研究所
老化ストレス応答研究プロジェクトチーム
Mail:shimizut(at)ncgg.go.jp ((at)を@に変えてください)
電話:0562-44-5651 (内7363 or 6101)
先頭へ戻る



 本研究の成果は10月16日に富山大学と共同でプレスリリースを行いました。富山大学プレスリリース
本研究の成果は10月16日に富山大学と共同でプレスリリースを行いました。富山大学プレスリリース 、国立長寿医療センタープレスリリース
、国立長寿医療センタープレスリリース
 )がオンライン科学誌「Biomedicines」に掲載されました。
)がオンライン科学誌「Biomedicines」に掲載されました。







