健康長寿ラボ
英独蘭の欧州のグループは、100万人以上に及ぶデータから、健康寿命、親の寿命、長寿命に関連する遺伝子に関する統計情報を用いて、この3つすべてに影響を及ぼす遺伝子群を同定したことを報告しました1。これまでに数多くの表現型(※)(身長、血圧、病気のなりやすさから知的好奇心の高低、さらには学歴や肉の摂取量など)に関連する遺伝子が調べられています。この関連する遺伝子群の重複や類似性から、表現型同士の関連を算出するメンデルランダム化解析という方法を用いて、上記の3つの表現型すべてに最も高い関係を示したのがヘムの代謝でした。ヘムとはミトコンドリアで合成される鉄を中心とした鉄の輸送体で、ヘモグロビンやミオグロビンといった鉄タンパク質の活性を担います。ヘムの合成は加齢とともに低下して、そのため細胞内への鉄の蓄積や酸化ストレスの増加を引き起こします。血清の鉄の濃度が高いと3つの寿命が短くなり、逆に鉄に結合して酸化ストレスを抑えるトランスフェリンというタンパク質の濃度が高いと3つの寿命は伸びうると試算されました。この知見により、適切な鉄のコントロールが長寿命や健康寿命に関わる可能性が示されました。
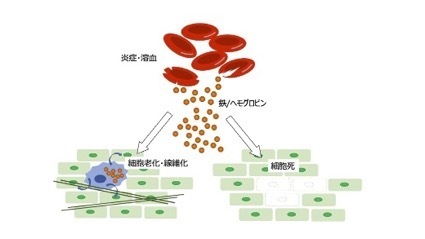
局所的な細胞外の鉄が、細胞の老化や組織の線維化の引き金になることも報告されています。スペインのSerrano博士のグループは、細胞や動物を用いた実験から、炎症やそれに伴う溶血により、赤血球から漏れ出したヘモグロビンや鉄が、細胞の老化や線維化を引き起こすことを見出しました2。局所的な鉄の増加は、全身レベル(血液など)の鉄の濃度と関係なく、線維化組織や老化細胞(※)に鉄の蓄積を招くことから、組織の線維化や老化の目印(マーカー)となる可能性も提案しています。また、薬剤による鉄の除去(キレートといいます)により、実験的な線維化も抑制されることも示しています。
この2つの研究からも、全身もしくは局所的な鉄の増加が寿命や細胞の老化などに関わる可能性を示しています。さらに最近では鉄に依存した細胞の死(フェロトーシスと呼ばれます)も明らかになっており、モデル実験のレベルですが、認知症や心疾患、関節疾患など、様々な加齢性の変性疾患に関係しているのではないか、という報告も増えてきています。このフェロトーシスと呼ばれる細胞死を抑制するのには、ビタミンKが有効ではないかとの知見も得られています3。最近の研究では、老化細胞は通常フェロトーシスを起こすような鉄の蓄積に対して耐性をもつようになっていることも報告されました4。
一方で、高齢者にもよく見られるのが鉄欠乏性貧血です。栄養障害や慢性出血が主な原因とされています。鉄の持続的な過剰状態も不足状態も健康にはよくありません。体内の鉄の状態や量の調節は重要で、諸刃の剣となりえるようです。
Timmers et al. Multivariate genomic scan implicates novel loci and haem metabolism in human ageing. Nature Commun. (2020) 11:3570.
Maus et al. Iron accumulation drives fibrosis, senescence and the senescence-associated secretory phenotype. Nature Metab. (2023) 5:2111-2130.
Mishima et al. A non-canonical vitamin K cycle is a potent ferroptosis suppressor. Nature (2022) 608:778-783.
Zhuang et al. Ageing limits stemness and tumorigenesis by reprogramming iron homeostasis. Nature (2025) 637:184-194.
表現型:観察・測定が可能な特徴や性質を指します。
老化細胞:老化した細胞で、近年の研究では、このような細胞が増えたり、炎症に関わる物質を分泌したりして老化に伴う疾患の発症や進展に関係するのではないかと考えられています。
文 渡邉研(運動器疾患研究部 )
)
![]()