プレスリリース
~アルツハイマー病の神経細胞死のメカニズムについての考察~
2026年2月19日
国立研究開発法人 国立長寿医療研究センター
国立研究開発法人国立長寿医療研究センター(理事長:荒井秀典。以下国立長寿医療研究センター)分子基盤研究部(部長:里直行)の研究グループは東京都健康長寿医療センター、大阪大学、中国香港科技大学との共同研究により、アルツハイマー病の進行期に脳内に蓄積する断片型Aβやタウの脳内の分布が、蛋白分解酵素であるカテプシンやジペプチジルペプチダーゼの脳内の分布とよく類似することを発見し、その成果をActa Neuropathologica Communicationsに発表しました。
アルツハイマー病患者の脳内では、老人斑として蓄積するAβ(注1)や神経原線維変化として蓄積するタウ(注2)といったタンパク質の蓄積が病気の発症に関与していると考えられていますが、なぜそれらのタンパク質が蓄積するのか、またそれらの蓄積がどのように神経細胞死に結び付くのか十分には分かっておりません。
これまでの我々などの研究により、病初期から蓄積するAβ1-42(以下、全長型Aβ42)の分布は前頭葉や線条体といった脳部位を中心に蓄積し神経シナプス(注3)に関連する分子の脳内の分布とよく類似することから、Aβの蓄積開始には何らかの神経機能が関与するとみられています。その一方で、疾患の進行とともに増加するN末端(注4)が断片化されたAβt-42(以下、断片型Aβ42)は、脳の辺縁系を中心に蓄積し、タウの脳内の分布と類似することが分かっています。すなわち断片型Aβ42の分布は病態進行を理解する手がかりと考えられます。また進行期ではC末端(注4)が短いAβ40などの分子も蓄積しますが、その分布は十分に検討されていませんでした。
本研究では、東京都健康長寿医療センターで保管している剖検脳をあらたに用いて、全長型Aβ42と神経シナプスに関連する分子であるPSD95とシナプトフィジン(SYT1)の脳内の分布をELISA法(注5)で測定すると、病初期から高い相関係数(注6)を示す、つまりそれらの分布が類似していることをまず再確認しました(図1)。
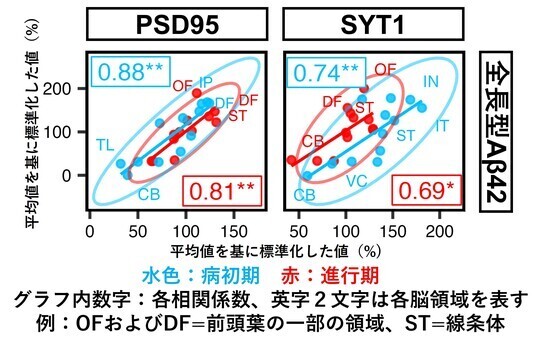
図1.全長型Aβ42とシナプス関連分子PSD95およびSYT1の脳内分布の類似性
一方で病態進行の手掛かりである断片型Aβ42の分布と類似する可能性のある分子として、蛋白分解酵素(注7)であるカテプシン(注8)やジペプチジルペプチダーゼ(注9)に着目して、それら関連分子の発現を測定しました。すると、カテプシンやジペプチジルペプチダーゼの多くがアルツハイマー病患者脳内で類似した分布を示すようになること、中でもカテプシンB(CatB)やカテプシンD(CatD)、ジペプチジルペプチダーゼIV(DPPIV)の分布がともに、進行期において断片型Aβ42やC末端の短いAβ40、タウの分布と強い相関係数を示し、よく類似することが分かりました(図2)。
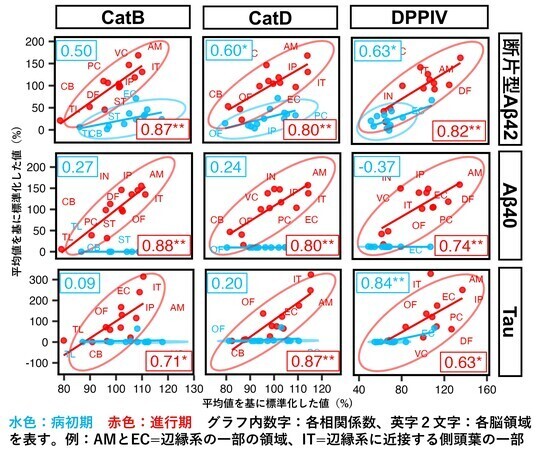
図2.断片型Aβとタウおよび蛋白分解酵素の分布の類似性(CatB:カテプシンB、CatD:カテプシンD、DPP-IV:ジペプチジルペプチダーゼIV、Tau:タウ)
また病理組織染色(注9)の検討からも、これらカテプシンやジペプチジルペプチダーゼはAβやタウの蓄積周囲に異常発現がみられることが確認できました(図3)。
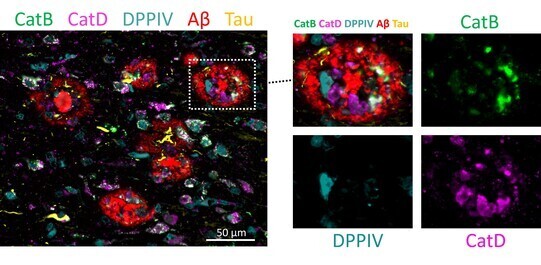
図3.アルツハイマー病患者脳内でのカテプシンやジペプチジルペプチダーゼの異常発現(右側の拡大図で示しているのは、赤色のAβコア(中心核)の周囲に、CatB(緑色)やDPPIV(シアンブルー色)、CatD(紫色)が通常とは異なる形で存在する様子である。タウ蓄積(黄色)もその近傍に存在することが分かる)
本研究から推測されることとして、まず病初期には全長型Aβ42が蓄積しますが、そのことは神経機能がその蓄積開始に関与すること。一方で病気の進行とともに断片型Aβ42が辺縁系を中心に蓄積していきますが、カテプシンやジペプチジルペプチダーゼが最初に蓄積した全長型Aβ42の断端(N末端ならびにC末端)に対する修飾分解を行うとともに神経細胞死にも寄与する可能性があると考えられます。
本研究結果は、あくまで患者脳内で認められた相関性であり、直接因果関係を示すようなデータではないため、今後はさらにそれらの因果関係(カテプシンやジペプチジルペプチダーゼが脳内でどのように全長型Aβ42の修飾分解や神経細胞死に寄与するか等)を証明するための実験などを行い、研究をすすめていく予定です。カテプシンやジペプチジルペプチダーゼが神経細胞死に寄与するのであれば、これら分解酵素を阻害する薬剤が、アルツハイマー病の新しい治療薬になり得ます。また今回の分解酵素に加えて断片型Aβ42やタウと領域相関する新しい分子を見出しています。患者さんの脳内におけるそれらの役割を理解することで認知症の神経細胞死のメカニズムの解明に迫れる可能性があることから、今後も脳内の病的蛋白質の分布に注目した研究を続けていきます。

図4.全長型Aβ42(Aβ1-42)や断片型Aβ42(Aβt-42)およびAβ40の模式図
Mitsuru Shinohara, Ghupurjan Gheni, Kaori Kawai, Maho Morishima, Shigeo Murayama, Yuko Saito, Guojun Bu, Naoyuki Sato. Coordinated Regional Association of Cathepsins and Dipeptidyl Peptidases with N-truncated Abeta42, Abeta40, and Tau in Alzheimer’s Brain. Acta Neuropathologica Communications, Volume 14, article number 31, (2026), doi: 10.1186/s40478-025-02146-1.
国立長寿医療研究センター研究所 認知症先進医療開発センター
分子基盤研究部 部長 里直行、副部長 篠原充
電話:0562-46-2311(代表)E-mail:nsato(at-mark)ncgg.go.jp
国立長寿医療研究センター総務部総務課 総務係長(広報担当)
〒474-8511 愛知県大府市森岡町七丁目430番地
電話:0562(46)2311(代表)E-mail:webadmin(at-mark)ncgg.go.jp
※(at-markを「@」に置き換えてください)
![]()