プレスリリース
ホーム > 研究所 > 研究実績 > アルツハイマー病の早期診断血液バイオマーカーとして注目されるタンパク質が記憶の形成に関わる神経細胞のシナプス損傷を反映していることをモデルマウスの解析から明らかにしました
2022年11月07日
国立研究開発法人 国立長寿医療研究センター
国立研究開発法人国立長寿医療研究センター(理事長:荒井秀典)・研究所・認知症先進医療開発センター・神経遺伝学研究部の廣田 湧 研究員,飯島浩一 部長,関谷倫子 副部長らは,アルツハイマー病を発症する前段階のプレクリニカル期から,血液や脳脊髄液中で増加するリン酸化タウタンパク質が,記憶の形成に重要な神経細胞のシナプスの損傷を反映していることを明らかにしました。
認知症の最大の原因であるアルツハイマー病は,脳実質へのアミロイドβの蓄積(アミロイド病理)と,神経細胞内へのリン酸化タウタンパク質の蓄積(タウ病理),そして神経細胞死による脳萎縮を特徴とする進行性の神経変性疾患です。近年,脳内のアミロイド病理やタウ病理を観察できる脳画像解析法(ポジトロン断層法)や,脳脊髄液中のアミロイドβやタウタンパク質を測定するバイオマーカーなどの開発により,アルツハイマー病を発症する前に診断することが可能になりつつあります(図1)。しかし,脳画像解析には特別な設備が必要でコストも高く,脊髄穿刺による脳脊髄液の採取は身体的負担が大きいことが問題になっていました。そこで,身体的負担が小さくかつ低コストでアルツハイマー病を早期に検出する方法として,血液バイオマーカーの開発が世界中で進められています。最近,脳にアミロイド病理を蓄積している,アルツハイマー病発症前からアルツハイマー病初期の患者さんの血液中で,リン酸化タウタンパク質の量が上昇することが報告され,アルツハイマー病を早期に診断するための血液バイオマーカーとして大きな注目を集めています。
タウタンパク質は神経細胞の軸索に局在し,細胞骨格である微小管の安定化や軸索輸送等に関与しています。タウタンパク質の正常なリン酸化はそれらの生理機能に関わりますが,アルツハイマー病患者さんの脳では過剰にリン酸化を受けて神経細胞の中に蓄積し,また一部のリン酸化タウタンパク質は断片化されて,脳脊髄液中や血液中で検出されることが知られています。近年,初期のアルツハイマー病を検出するリン酸化タウタンパク質が相次いで報告され,中でも181,217,231番目のスレオニン残基がリン酸化されたタウタンパク質(以下,pT181タウ,pT217タウ,pT231タウ)は,アルツハイマー病を高い精度で鑑別診断します(図1)。また興味深いことに,pT217タウとpT231タウは,pT181タウよりも高い感度でアルツハイマー病の発症前,初期段階を検出できることも報告されています。これらのリン酸化タウタンパク質は,アルツハイマー病の初期に起こる脳の病的な変化と関係していると考えられますが,具体的にどのような脳の病態を反映しているのかは明らかではありませんでした。
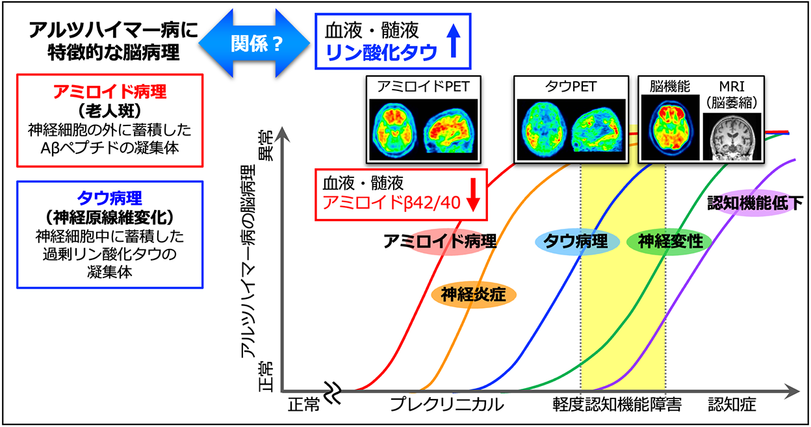
図1.アルツハイマー病の脳病理の変化とバイオマーカーリン酸化タウタンパク質
今回,廣田らは,アルツハイマー病発症前から初期のアミロイド病理を再現するアミロイド病理モデルマウス(Appノックインマウス,参考文献1,2)を用いて,血液バイオマーカーであるpT181タウ,pT217タウ,pT231タウが,脳内のどのような病変を反映しているのかを調べました。その結果,pT217タウとpT231タウは,正常なマウスの脳には存在せず,アミロイド病理モデルマウスの脳内のみに出現し,アミロイド病理が引き起こすシナプス後部の変性を反映していることを見出しました(図2A)。一方pT181タウは,正常なマウスの脳の神経細胞の軸索に存在しますが,アミロイド病理モデルマウスでは,アミロイドβ斑の周囲でそれらの軸索が変性していることを見出しました(図2B)。以上の結果から,アルツハイマー病の発症前から検出されるバイオマーカーリン酸化タウタンパク質のpT217タウとpT231タウは,記憶の形成に重要な興奮性神経細胞のシナプス後部の異常を,pT181タウは神経伝達に必要な神経細胞の軸索の異常を反映している可能性が示されました(図3)。
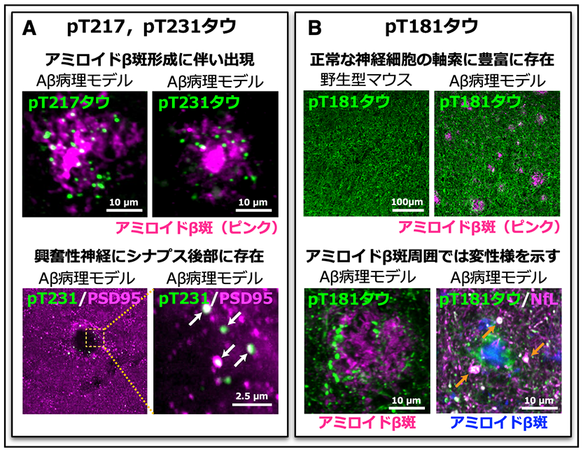
図2.アミロイドβ病理モデルマウス脳でのバイオマーカーリン酸化タウタンパク質の局在
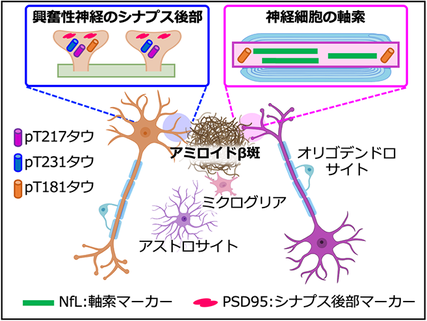
図3.アミロイドβ斑周囲のリン酸化タウタンパク質の局在
本研究では,アルツハイマー病の発症前・初期の過程で,脳脊髄液や血液中で増加するリン酸化タウタンパク質が反映する脳病態を明らかにしました。今回解析を行ったバイオマーカーリン酸化タウタンパク質と同様に,アミロイドβ斑の周囲で変化するタンパク質は,アルツハイマー病発症前の新しい血液・脳脊髄液バイオマーカーになる可能性があります。本研究結果を基に,アルツハイマー病の脳病態のさらなる解析を行い,新たなバイオマーカーの発見・開発に貢献したいと考えます。
本研究成果は,令和4年11月7日付けで科学誌Brain Communicationsのオンライン版に掲載されました。なお,本研究は国立長寿医療研究センター長寿医療研究開発費,科研費(日本学術振興会科学研究費助成事業)からの研究助成を受けて行われました。
Yu Hirota, Yasufumi Sakakibara, Kyoko Ibaraki, Kimi Takei, Koichi M. Iijima, Michiko Sekiya, “Distinct brain pathologies associated with Alzheimer’s disease biomarker-related phospho-tau 181 and phospho-tau 217 in App knock-in mouse models of Aβ amyloidosis” Brain Communications, 2022, doi: 10.1093/braincomms/fcac286
https://academic.oup.com/braincomms/advance-article/doi/10.1093/braincomms/fcac286/6795489
国立長寿医療研究センター総務部総務課広報担当 総務係長 伊藤
〠474-8511 愛知県大府市森岡町七丁目430番地
電話 0562(46)2311(代表) E-mail:d-ito5963@ncgg.go.jp
国立長寿医療研究センター研究所・認知症先進医療開発センター
神経遺伝学研究部 副部長 関谷 倫子,部長 飯島 浩一
電話 0562(46)2311(内線 6402/6408) E-mail:mmsk@ncgg.go.jp
![]()