研究実績
2021年04月06日
国立研究開発法人国立長寿医療研究センター
脳血管性認知症は認知症の中でもアルツハイマー病に次いで多い疾患ですが、血管病変がどのような機序で認知機能低下をもたらすか、詳しくは分かっておりません。今回、脳血管障害時に発現増加する遺伝子の一つを欠損するマウスを作成し、行動異常が増悪するとともにグリア細胞1)の増殖がより顕著になることを米国の専門誌に報告しました。この結果は、Journal of Neuroinflammation誌に2021年4月4日付(JST)で掲載されました。
今回、国立長寿医療研究センター(理事長:荒井秀典)の認知症先進医療開発センター、分子基盤研究部の鈴木香研究員、篠原充副部長、里直行部長のグループは三重大学の冨本秀和教授、大阪大学の真下知士 現東京大学教授らとの共同研究により、B cell translocation gene-2 (Btg2)遺伝子を欠損するマウスを作成し、さらにその脳血流障害モデルを解析しました。その結果、Btg2遺伝子を欠損するマウスでは脳血流を障害した場合、オープン・フィールド試験における総移動距離が有意に増加することが判明しました(図1)。さらに脳の白質2)においてアストロサイト3)および単球4)・マクロファージ5)のマーカーが増加していました(図2)。
この遺伝子「Btg2遺伝子」は脳血管障害時だけでなく、われわれが最近報告した、肥満・糖尿病を合併したアルツハイマー病モデルにおいても発現増加する遺伝子群6)クラスター7)10の一つであることから(参考文献)、神経変性に共通した因子である可能性があります。また、Btg2遺伝子を欠損したアストロサイトでは炎症刺激時における細胞増殖がより増加していたことから、Btg2遺伝子は炎症刺激時における細胞増殖に対し、抑制的に働く可能性が示唆されました。
クラスター10に属する遺伝子の病気における役割はまったく分かっていませんでしたが、今回のわれわれの研究によってその一端を明らかにしたことになります。今後、さらに、これらの遺伝子の機能解析を進めることにより、アルツハイマー病や脳血管性認知症の病態が明らかとなり、その結果として認知症に対する創薬につながることが期待されます。
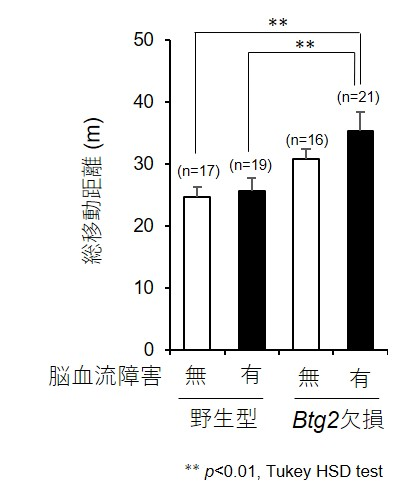
図1.オープン・フィールド試験
30cm立方ケージにおける15分間の自由行動下での移動距離を測定。Btg2欠損マウスでは脳血流障害時の総移動距離が増加。
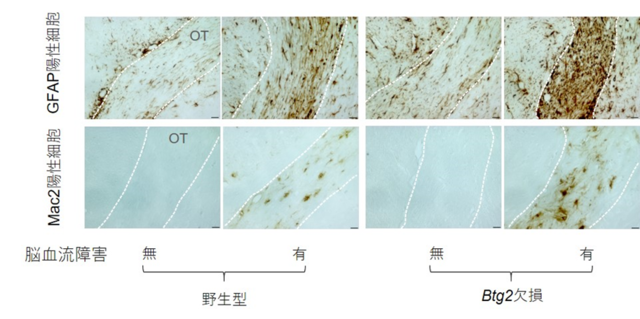
図2.白質におけるアストロサイト・マクロファージの活性化
アストロサイトのマーカーであるGFAP(Glial Fibrillary Acidic Protein)および単球・マクロファージのマーカーであるMac2の免疫染色像(茶色部分が陽性細胞)。Btg2欠損マウスでは脳血流障害時のアストロサイトと単球・マクロファージのマーカーの発現が顕著に増加している。
OT: Optic Tract8) 、視索(白点線内側)、スケール、20 mm。
URL:https://faseb.onlinelibrary.wiley.com/doi/10.1096/fba.2020-00151
♯筆頭著者、*責任著者
URL:https://jneuroinflammation.biomedcentral.com/articles/10.1186/s12974-021-02135-w
*責任著者
国立研究開発法人国立長寿医療研究センター
認知症先進医療開発センター分子基盤研究部長 里直行
〒474-8511 愛知県大府市森岡町七丁目430番地
電話 0562(46)2311(内線6331) E-mail:nsato@ncgg.go.jp
国立長寿医療研究センター総務部総務課総務係長 里村亮
電話 0562(46)2311(内線4623) E-mail:r-satomura@ncgg.go.jp
![]()