News & Topics
ホーム > 病院 > 先端医療開発推進センター > ニュース&トピックス > AI技術SOLPCS(ソルピクス)によるアルツハイマー型認知症の進行予測


AI技術SOLPCS(ソルピクス)によるアルツハイマー型認知症の進行予測
ー短期間の認知機能データで長期的な認知機能変化を予測、早期診断・治療・臨床試験の効率化に貢献ー
2025年4月7日
東京科学大学
国立長寿医療研究センター
東京科学大学(Science Tokyo)大学院医歯学総合研究科 臨床統計学分野の佐藤宏征講師、花澤遼一大学院生、平川晃弘教授らの研究チームは、国立長寿医療研究センターの鈴木啓介センター長、名古屋大学の橋詰淳講師と共同で、短期間の認知機能テストデータをもとに自己組織的に予測モデルを構築し、長期的な認知機能の変化を予測するAIアルゴリズム「Self-Organized Longitudinal Prediction-Classification-Superposition(SOLPCS、ソルピクス)」を開発しました。
アルツハイマー病(Alzheimer's Disease; AD)は、数十年にわたり進行する認知機能低下を特徴とする神経変性疾患であり、早期発見と適切な介入が極めて重要です。しかし、AD発症前の健康な人の認知機能を長期間追跡し続けることは困難であるため、短期間の認知機能データを用いて長期的な変化を正確に予測する方法が求められています。
SOLPCSの予測精度について、ADに関する大規模研究である米国のAlzheimer’s Disease Neuroimaging Initiative(ADNI、用語1)研究および日本のJapanese ADNI(J-ADNI、用語2)研究のデータを用いて検証した結果、高精度な予測が可能であることが確認されました。さらに、SOLPCSを応用することで、①アルツハイマー型認知症の発症および進行に関わるリスク因子を同時に特定すること、②AD治療薬の臨床試験における成功確率を向上させる可能性が示されました。
SOLPCSは、アルツハイマー型認知症の早期診断や進行予測、さらにはAD治療薬の臨床試験の精度向上を通じて、社会全体の認知症予防や新薬開発の効率化に貢献することが期待されます。今後の展開として、近年普及が進むスマートフォンやタブレットを活用したセルフ認知機能テストやPersonal Health Record (PHR)データの予測への応用も視野に入れています。
本成果は、2月26日付(現地時間)で「IEEE Journal of Biomedical and Health Informatics」誌に掲載されました。
アルツハイマー病(Alzheimer's Disease; AD)は、長期にわたる認知機能低下を特徴とする神経変性疾患です。発症前の早期介入が進行を遅らせる可能性がありますが、健康な人の認知機能を20から30年にわたって追跡することは困難です。そのため、2から3年の短期間データから長期的な変化を予測する手法が求められています。
従来の予測手法には、非線形混合効果モデル(用語3)を用いる方法や統計モデルと微分方程式(用語4)を組み合わせた方法(Hirakawa et al., Statistics in Medicine, 2022、特願2022-084152)があります。しかし、これらは集団全体に共通の疾患進行パターンを仮定しており、ADの進行速度に個人差があることを考慮できません。その結果、急速に進行するケースと緩やかに進行するケースの違いを反映できず、予測精度が低下する可能性があります。
本研究では、これらの課題を解決するため、Hirakawaら(Statistics in Medicine, 2022、特願2022-084152)の手法を拡張し、短期間の認知機能データをもとに自己組織的に予測モデルを構築するAIアルゴリズム「Self-Organized Longitudinal Prediction-Classification-Superposition(SOLPCS、ソルピクス)」を開発しました。SOLPCSは、疾患進行パターンを分類し、それに基づいた予測を行うとともに、個人の認知機能テストの実測データを重ね合わせることで、より精度の高い個別化予測を可能にします。
SOLPCSの予測精度について、米国のAlzheimer’s Disease Neuroimaging Initiative (ADNI)研究および日本のJapanese ADNI(J-ADNI)研究のデータを用い、以下の認知機能テストで検証しました。
図1はADNI研究およびJ-ADNI研究におけるアミロイドβ(Aβ、用語5)陽性集団を対象にSOLPCSを適用した結果です。疾患進行パターンとして疾患低下速度が緩徐型、中等度型、急速型の3パターンに分類し、それぞれに対して長期的な認知機能変化を予測した結果が黒、青、赤の実線になります。破線は、個人の実際の認知機能テストデータを重ね合わせたものを表します。SOLPCSは各認知機能テストにおいて最大値の約10%以内の誤差(MMSE:3点以内、CDR-SOB:1.8点以内、ADAS-Cog:8.5点以内)で長期的な認知機能の変化を予測できることが確認され、臨床応用の可能性が示されました。
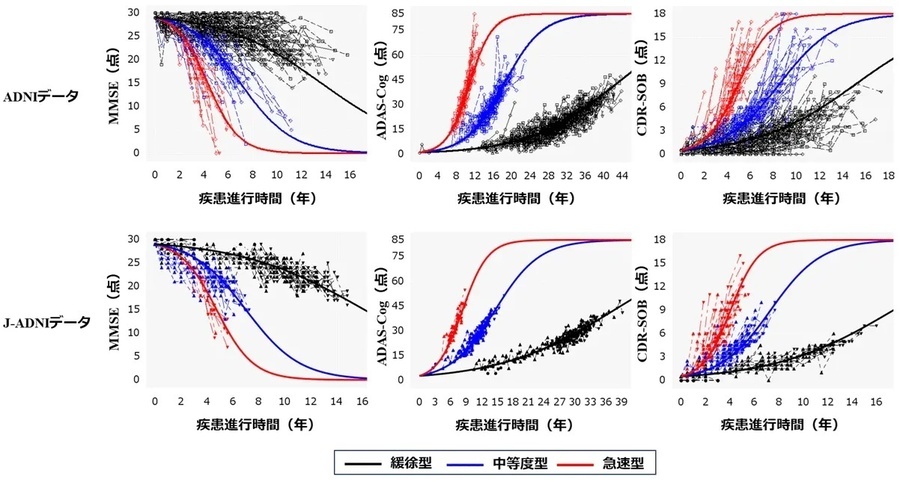
図1 ADNIおよびJ-ADNIデータを用いたSOLPCSの予測結果
SOLPCSを用いてアルツハイマー型認知症のリスク因子を解析し、APOE(アポリポプロテインE)ε4遺伝子(用語6)がアルツハイマー型認知症発症および進行に与える影響を評価しました。
結果として、Aβ陽性かつAPOE ε4陽性の軽度認知障害(MCI)の方は、Aβ陽性・APOE ε4陰性の方よりもアルツハイマー型認知症発症が有意に早いことが明らかになりました。また、APOE ε4遺伝子がアルツハイマー型認知症の進行に与える影響についても解析を行ったところ、本手法で得られた知見は、既存のシステマティックレビューの結果と一致しました。
近年、MCIや早期アルツハイマー型認知症を対象とした新薬開発のためのランダム化比較試験(用語7)が増加しています。しかし、多くのAD治療薬の臨床試験では、治療群とプラセボ群の間で統計的に有意な差を検出できないという課題があります。その要因の一つとして、登録患者の認知機能低下速度にばらつきが大きく、治療効果の評価が困難になることが挙げられます。
本研究では、SOLPCSを用いて試験登録時に各参加者の認知機能の長期的な変化を予測し、進行速度が極端に遅いまたは早い患者を除外する試験デザインを開発しました。AD治療薬の臨床試験を想定したクリニカルトライアルシミュレーション実験(用語8)の結果、この方法によりデータのばらつきを抑え、統計的検出力を向上させることが確認されました。これにより、AD治療薬の臨床試験の成功確率が向上することが期待されます。
ADは進行性の神経変性疾患であり、高齢化が進む社会において早期発見と適切な介入が重要な課題です。しかし、現在の診断には高額な検査や専門医の診察が必要であり、早期診断の機会が限られています。
本研究で開発したSOLPCSは、高額かつ高度な医療データを必要とせず、一般の医療機関や定期健康診断の場でも長期的な認知機能の変化を評価できる可能性を広げます。また、認知症の発症や進行に関連するリスク因子を特定し、個別に適した予防策の提案が可能になります。例えば、生活習慣の改善(運動・食生活の見直し・脳トレなど)を通じて、リスクの高い人への早期介入が実現し、社会全体の認知症予防に貢献すると期待されます。
さらに、AD治療薬の開発においても、SOLPCSを活用することで、認知機能低下速度が均質な患者集団を対象とした臨床試験が可能になり、臨床試験の成功確率を向上させることができます。これにより、新薬の実用化が加速し、認知症治療の進展に大きく貢献すると期待されます。
本研究で開発したSOLPCSは、早期診断・予防・治療の各フェーズでの応用が期待されるAIアルゴリズムですが、社会実装にはさらなる発展が必要です。現在、スマートフォンやタブレットを活用したセルフ認知機能テストが普及しつつあり、SOLPCSと組み合わせることで、より手軽な認知症リスク評価システムの開発が可能になります。
具体的には、スマートフォン上で認知機能テストを行い、そのデータをSOLPCSに入力することで、個人ごとの長期的な認知機能変化を予測するAIアプリを開発します。このアプリは、予測結果に基づいた個別の認知症予防策(食事・運動・脳トレ等)を提案し、ユーザーの行動変容を促すことを目指します。さらに、自治体や企業の健康増進プログラムと連携し、地域全体での認知症予防に活用することも可能です(図2)。
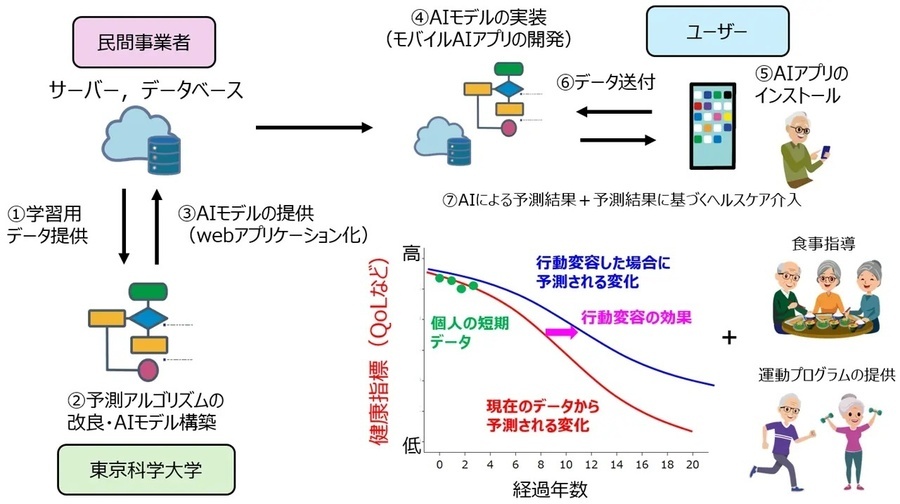
図2 AIアプリの社会実装と長期的認知機能予測結果に基づいたヘルスケア介入
今後は、近年普及が進むスマートフォンやタブレットを活用したセルフ認知機能テストやPersonal Health Record(PHR)データの予測にも応用し、一般市民も手軽に健康状態を把握できる社会の実現を目指します。
アルツハイマー病の進行に関するデータを収集・提供する、米国の大規模な研究プロジェクト。脳画像、認知機能検査、バイオマーカーなどのデータを蓄積している。記事へ戻る
日本版ADNIで、日本国内のアルツハイマー病研究のために収集されたデータベース。ADの早期診断技術の開発や病態解明を目的としている。記事へ戻る
個人ごとのデータのばらつきを考慮しながら、集団全体の傾向を推定する統計モデル。医療や生物統計の分野で、個人差を考慮した解析に用いられる。記事へ戻る
変数の変化の割合を記述する数式。病気の進行や薬の効果など、時間とともに変化する現象のモデリングに用いられる。記事へ戻る
アルツハイマー病の主要な病理マーカーとされるタンパク質。脳内に蓄積し、神経細胞の障害を引き起こすと考えられている。記事へ戻る
アルツハイマー病の発症リスクを高める遺伝的要因の一つ。記事へ戻る
新しい治療法の有効性を検証するための臨床試験の標準的な方法。参加者をランダムに治療群と対照群に分け、治療効果を客観的に評価する。記事へ戻る
臨床試験の成功確率を最大化するために実施されるコンピュータシミュレーション実験。疑似的な患者データをコンピュータ内で生成・分析することで、想定される薬剤の効果、登録可能な患者数、試験期間、データ解析に用いる統計解析法など、臨床試験の計画、実施に係る諸条件を最適化できる。記事へ戻る
IEEE Journal of Biomedical and Health Informatics
Self-Organized Prediction-Classification-Superposition of Longitudinal Cognitive Decline in Alzheimer’s Disease: An Application to Novel Clinical Research Methodology
Hiroyuki Sato, Ryoichi Hanazawa, Keisuke Suzuki, Atsushi Hashizume, Akihiro Hirakawa
東京科学大学 大学院医歯学総合研究科 臨床統計学分野 講師
臨床統計学、臨床試験方法論、データサイエンス
東京科学大学 大学院医歯学総合研究科 臨床統計学分野 大学院生(博士課程)/ 東京科学大学病院 ヘルスサイエンスR&Dセンター 特任助教
臨床統計学、臨床試験方法論、データサイエンス
国立長寿医療研究センター 先端医療開発推進センター センター長
ライフサイエンス、神経内科学、認知症
名古屋大学 大学院医学系研究科 臨床研究教育学 講師
ライフサイエンス、神経内科学
東京科学大学 大学院医歯学総合研究科 臨床統計学分野 教授
臨床統計学、臨床試験方法論、データサイエンス
東京科学大学 大学院医歯学総合研究科 臨床統計学分野 教授 平川晃弘
Email:a-hirakawa.crc@tmd.ac.jp
東京科学大学 総務企画部 広報課
Email:media@adm.isct.ac.jp TEL:03-5734-2975 Fax:03-5734-3661
国立長寿医療研究センター 総務部総務課 総務係長(広報担当)
Email:webadmin@ncgg.go.jp TEL:0562-46-2311
迷惑メール防止のため、@を全角表示しております。メール送信にあたっては、半角の@に直してお送りください。